从衣壳工程化的开发过程来看,首先要选取一个理想的工程化改造位置,然后通过特定的改造手段围绕着野生型AAV衣壳产生个性化的改造内容。
因此,不管是理性设计中在细胞受体结合关键区域插入靶向性肽,亦或是对胞内降解相关的关键氨基酸残基进行突变,还是定向进化改造中通过在特定位置插入多种随机肽来建库,早期改造位置相关的发明是后续工程化的基础。换句话说,围绕着工程化改造位置相关的风险(即,I类风险),是衣壳工程化领域内的基础专利风险障碍。从规避难度上讲,基础风险障碍通常是由领域内早期开拓者设置的一类非常宽泛的风险障碍,这部分专利通常会涉及核心技术原理或机理,相对来说难以绕开。比如基因编辑领域的CRISPR/Cas9系统,张锋和Jennifer A.Doudna等人设置的专利壁垒使后续想要使用该系统在真核细胞中进行编辑的玩家非常棘手。
对于工程化改造内容相关的发明(即,II类风险),比如靶向性的肽、衣壳变体序列,保护范围相对来说较窄,属于更下位的风险障碍,理论上技术规避的空间更大。而工程化改造手段来源的风险(即,III类风险)包括诸如定向进化中不同的建库和筛选方法之类的发明,企业是否面临这类风险带来的障碍,取决于是否会利用这些方法自主开发工程化衣壳。
目前大部分基因治疗Biotech往往会直接选择领域内现有或已经验证的工程化衣壳,因此下面我们将主要探讨I类和II类风险的障碍情况。我们认为,落实到具体的工程化衣壳中,当使用不同的工程化改造位置或改造后的应用于不同的疾病领域,这两类风险带来的障碍会存在区别。
I类风险差异
在I类风险中,工程化改造位置“细胞受体结合关键区域”和“胞内降解关键氨基酸残基”带来的基础风险障碍大小存在差异。
作为决定“能不能进入”的重要影响因素,衣壳蛋白上的细胞受体结合关键区域首先被探索。在早期,凭借着对AAV衣壳蛋白结构的初步认识,领域内尝试对衣壳蛋白表面的区域进行修饰,以确认哪些区域在决定AAV衣壳能够结合特定细胞受体中扮演着重要角色。随着2002年AAV2血清型三维结构的揭示,以及后续Michael S. Chapman团队和Mavis Agbandje-McKenna团队陆续对其他常用血清型,如AAV8、AAV9和AAV5结构的解析,AAV衣壳蛋白上细胞受体结合关键区域进一步得到确认。
目前普遍认为,AAV衣壳蛋白结构中三倍凸起区域在AAV衣壳能否结合特定细胞受体中扮演着重要角色,因此在三倍凸起区域的暴露氨基酸残基处插入靶向性的肽,以重塑或提高对特定细胞的转导效率,是目前衣壳工程化领域的热门策略。
AAV2是目前临床应用最广泛的AAV血清型,通过与细胞表面的硫酸乙酰肝素蛋白聚糖(HSPG)相互作用从而实现细胞转导,而决定其与HS结合的关键氨基酸残基主要为R484,R487,K532,R585和R588,其中R585-R588区域至关重要,这也就是为什么后来领域内基本集中在587位进行改造。
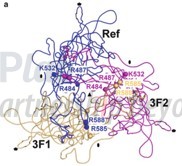
早在1999年MICHAEL HALLEK等人就在这些位点附近尝试通过插入靶向性肽从而试图改变AAV2的靶向性,PCT/EP1999/004288公开在447、534、573和587位等进行尝试后,发现在587位插入一段整合素靶向性的肽之后,能够使AAV2对表达整合素受体的细胞具有靶向性,而野生型AAV2并不能感染该细胞。这一发现也在2002年AAV2的高分辨率结构解析结果中进一步得到确认。
家族成员EP1088075B1保护“对衣壳蛋白进行突变修饰,使其能够在形成病毒粒子的情况下提高转导效率”这一概念,US7314912B1保护优势位点587。所有家族成员均已于2019年到期失效。这也就意味着后续所有使用在587位点插入靶向性肽进行改造的工程化AAV衣壳,将不会再有来自该位点层面的宽泛风险。

衣壳蛋白三维结构的确定,为通过改造细胞受体结合关键区域以开发高效转导特定细胞或组织的工程化AAV衣壳提供了基础。在2010年左右,常用血清型的衣壳蛋白结构基本解析出来,这也就意味着影响AAV能不能进入的细胞受体结合的关键区域大概率已经得到充分的探索。
相较于受体结合关键区域,领域内更晚发现,衣壳蛋白表面某些氨基酸会因为某些机制引发进入胞内的AAV降解。最早在2008年左右,来自佛罗里达大学的Arun Srivastava等人首次发现,在EGFR-PTK作用下AAV衣壳表面暴露的酪氨酸残基(Y)会被磷酸化,进而引发泛素化介导的蛋白酶降解。随后又陆续发现特定位置的丝氨酸(S)、苏氨酸(T)和赖氨酸(K)也会发挥相同的作用。
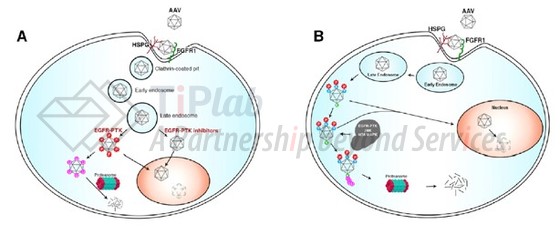
PCT/US2008/059647家族就是保护影响胞内降解的关键酪氨酸残基Y252,Y272,Y444,Y500,Y700,Y704和Y730,其中变体Y444F,Y500F和Y730F效果最优。家族成员US10723768B2保护上述关键位点,US9775918B2保护单个位点。后续家族PCT/US2009/044753成员保护三个最优效果位点的组合。

从机理发现的先后顺序可以看出,领域内较早开展对衣壳蛋白中受体结合关键区域的探究,2008年左右才开始对影响胞内降解酶的关键氨基酸进行解析,因此类似PCT/US2008/05964家族的专利到期日也会相对更晚,那么利用影响胞内降解酶的关键氨基酸为基础的工程化改造整体风险会相对更大。并且在这类风险中,因为丝氨酸(S)、苏氨酸(T)和赖氨酸(K)发现相较酪氨酸(Y)更晚,相应的专利障碍会更晚到期。
II类风险差异
除了工程化改造位置相关的基础风险障碍,使用工程化AAV衣壳还需要考虑改造内容相关的风险障碍。
改造内容相关的风险专利因为限定到具体插入肽的序列或者修饰的氨基酸的类型,技术上存在一定的规避空间,可以考虑对序列进行略微修饰或者选择不同的氨基酸类型,从而获得新的AAV衣壳变体。
当然,规避空间也和针对特定疾病领域的工程化衣壳研究是否拥挤有关,如果衣壳工程化开发在某类疾病领域尤其活跃,那么该赛道上的玩家已经充分地探索了可行的工程化衣壳,与之产生的各种可行的改造内容相关的发明大概率会得到充分保护。在这种情况下,对于想要通过微调序列规避风险障碍的Biotech来说,可能会面临很难找到一条效果可行且还没有被专利保护的序列。
我们可以以目前广泛应用到临床管线、对视网膜细胞具有高效转导效率的AAV7m8为例,其相关的专利资产主要涉及优势靶向性肽,其家族成员不仅保护了AAV7m8对应的优势肽,还保护了多条其他可选的肽段。对于想要通过改变AAV7m8插入肽序列来规避的玩家来说,不仅需要规避一条肽段序列,可能需要同时考虑被该家族保护的其他所有序列。
在衣壳工程化领域,针对眼科和CNS疾病的AAV工程化改造尤为火热,过去几年,在这两个领域从事衣壳开发的企业与大制药厂或头部基因治疗企业建立合作的事件频频发生。
例如,衣壳开发领头企业Voyager,凭借其AAV衣壳开发平台—TRACER技术平台,相继和诺华、辉瑞达成协议,授予后者基于该平台发现的新型AAV衣壳在CNS相关靶点上的使用权益。该平台能够高效发现有效穿越血脑屏障(BBB),且在多种物种(包括非人类灵长类)中具有加强的CNS趋向性的AAV衣壳。
此外,还有Capsigen(TRADE™平台,和Biogen合作CNS和神经肌肉疾病领域)、Affinia(ART衣壳平台,CNS领域)、StrideBio(STRIVE™平台,和Sarepta、CRISPR Therapeutics合作CNS和神经肌肉疾病领域)、Capsida(CNS和眼科疾病特异性AAV衣壳开发平台,和AbbVie、CRISPR Therapeutics和Lilly子公司Prevail合作)、ViGeneron(vgAAV衣壳平台,和Biogen、第一三共和再生元合作眼科疾病领域)、Avista(scAAVengr平台,和罗氏合作视网膜疾病领域)、Dyno Therapeutics(CapsidMap™平台,和罗氏、诺华、Astellas、Sarepta等合作骨骼肌和心肌疾病领域)。当然,国内也已经有一些企业相继进入了衣壳工程化开发领域,凭借用于上述2个疾病领域的AAV衣壳筛选平台与基因治疗药物开发企业开展了合作。
从上述领域内的合作动态来看,在眼科和CNS赛道已经聚集了不少工程化衣壳开发企业。我们发现,不管是衣壳开发企业本身,还是其合作方,围绕利用其专有的衣壳开发平台筛选出来的、针对特定组织或细胞的工程化AAV衣壳,递交了大量的专利申请。因此,相较于其他拥挤程度较低的疾病赛道,处在这两个疾病领域的Biotech,面临的风险障碍也就更大。如果企业本身不具备高效的衣壳开发平台,直接选择现有的工程化衣壳,然后希望通过微调序列,来规避相关专利资产带来的障碍,在这两个疾病领域内技术层面可能会面临更大的难度。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
