非病毒载体递送技术的研究和开发在过去的十年中得到了广泛的发展,并由于最近几年非病毒核酸治疗产品的成功批准而受到很大的推动。
目前用于RNA递送的非病毒载体涉及多种类型,包括脂质纳米颗粒、聚合物纳米颗粒、无机纳米颗粒以及基于偶联物的核酸递送系统等,但因为在体内的毒性和有效性,大部分递送系统都处在临床前或临床研究阶段。
前面的系列文章中我们梳理了临床已验证的LNP递送系统和GalNAc递送系统,下面我们先总结这2种技术的一些基本情况。
临床已验证的递送技术
LNP递送系统
LNP递送系统作为COVID-19 mRNA疫苗的重要组成部分备受关注,该系统主要包括阳离子脂质、胆固醇、PEG-脂质及辅助脂质,其在有效保护mRNA并将其转运至细胞方面发挥着关键作用。
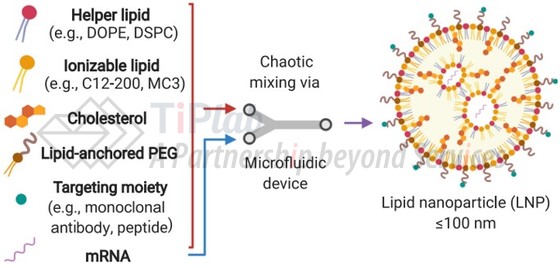
本系列文章二(阳离子脂质)讨论了阳离子脂质结构的优化过程,从最初的永久带电的脂质,过渡到如今广泛使用的可电离脂质和可生物降解脂质,都伴随着大量的专利布局。
本系列文章三(LNP组合物)中,我们讨论了LNP组合物的发现及专利保护情况,这部分内容也是研究LNP递送系统的企业,需要特别关注的,因为,LNP组合物中存在一部分未限定脂质组分结构仅限定各组分配比的有效专利,且部分配比制备的LNP组合物的稳定性及递送效率,在临床上已验证具备明显优势。
由此可见,对准备或已经进入LNP领域的企业来说,我们在进行风险排查时,需要同时分析来自阳离子脂质和LNP组合物各组分及其配比的潜在风险。
GalNAc递送系统
GalNAc递送系统,是GalNAc与肝脏实质细胞表面的去唾液酸糖蛋白受体(ASGPR)结合后,通过细胞内吞作用,进入到细胞内形成内涵体,从而将足够数量的核酸药物带入细胞内,实现核酸药物的肝靶向递送。
本系列文章四(GalNAc递送系统)中,我们讨论了三触GalNAc递送系统的结构特点及相应基础专利的情况,截止目前,该系统已有4款GalNAc-siRNA偶联产品获批上市,均由Alnylam开发。此外,还有多款衍生产品正处于临床研究阶段。

除典型的三触GalNAc递送系统,同样基于ASGPR/GalNAc原理构建的GalNAc递送系统,还有Dicerna 自主研发的包含单价GalNAc偶联的四环(tetraloop)结构的GalXC™平台,以及Arrowhead设计合成的包含高效RNA trigger的TRiM™。基于这两个平台,Dicerna和Arrowhead分别获得了来自诺和诺德、强生等企业的青睐,潜在交易金额高达数十亿美元,GalNAc递送系统未来前景十分可观。
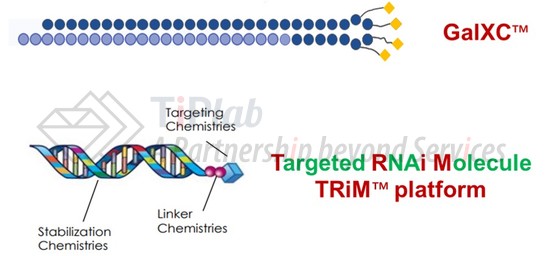
除上述LNP和GalNAc这2种已被临床验证的核酸药物递送系统,还有多种递送技术正处于临床研究阶段,包括:聚合物运载技术(Polyplexes,PPs)、脂质运载技术(Lipoplexes,LPX)、脂质多聚复合物(Lipopolyplexes,LPP)、抗体寡核苷酸偶联物(Antibody-oligonucleotide conjugates,AOC)、适配体核酸偶联物(ApDC)等。
临床正在验证的递送技术
下面,我们介绍2种临床正在验证的递送技术,抗体寡核苷酸偶联物(AOC)和脂质多聚复合物(LPP)。
抗体寡核苷酸偶联物
抗体寡核苷酸偶联物(AOC),是利用抗体将治疗性寡核苷酸(siRNA、ASO等)递送至特定的细胞或组织,其中,抗体部分通常被用作目标识别单元,而寡核苷酸部分则发挥多种治疗或检测功能。
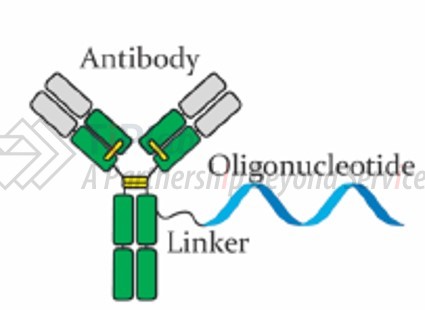
AOC是一种有前途的肝外组织药物靶向递送技术,可作为基因沉默抗癌剂或抗病毒剂、放疗增强剂,同时,还可作为研究抗体内化和代谢机制的工具。基于其应用前景较好,国内外已有多家企业或研究机构进入该领域。
AOC技术的先驱是Avidity Biosciences,早在2021年,该公司便将首款基于AOC技术开发的产品(AOC1001)推向临床。AOC1001由3部分组成:靶向转铁蛋白受体1(TfR1)的全长单抗、linker、靶向DMPK mRNA的siRNA,用于治疗强直性肌营养不良型1型(DM1)疾病。今年9月,由于1例严重副作用,FDA要求AOC1001的1/2期临床停止新患者入组。
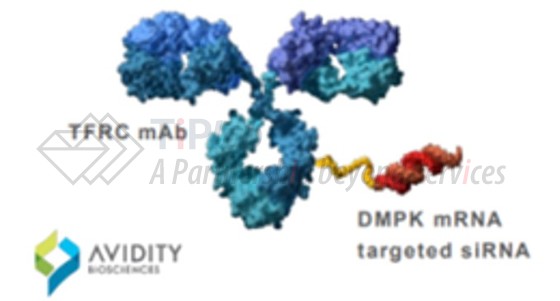
除Avidity Biosciences外,Dyne和Tallac也有AOC衍生产品进入I期临床,从两家公司近几年的融资来看,AOC技术吸引了诸多投资人的关注。
脂质多聚复合物(LPP)
脂质多聚复合物(LPP)是一种以聚合物包载mRNA为内核、磷脂包裹为外壳的双层结构。相比传统LNP具有更好的包载、保护mRNA的效果,并能够随聚合物的降解逐步释放mRNA分子。
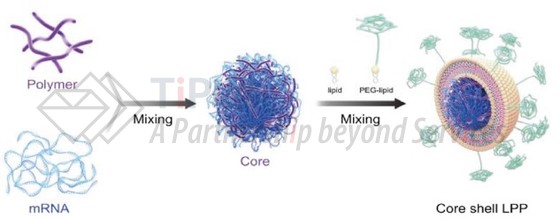
LPP递送系统,是将带正电的阳离子聚合物与带负电的mRNA分子紧密结合,形成一个被包裹在脂质壳中的致密核心结构(Core),然后,再将这个核和不同的脂质体混合形成核壳结构(Core shell LPP)。可见,LPP递送系统的制备过程与LNP递送系统存在明显的区别,LNP递送系统是将阳离子脂质、磷脂、胆固醇、PEG脂质各组分按特定比例和mRNA分子通过微流控技术混合(mix),伴随精准调节pH值和有机溶剂,形成目标LNP颗粒。
此外,由于LPP递送系统的整体结构类似于病毒,因此,它具有一些独特的优势,包括促进细胞摄取和刺激关键信号转导通路。该系统靶向树突状细胞效果优异,能够更好地通过抗原递呈激活T细胞的免疫反应,从而达到理想的免疫治疗效果。
LPP递送技术代表性的企业是斯微生物,针对该技术,斯微生物布局了相应的专利家族进行保护,目前已获得了包括美国、日本、欧洲在内的多个地域的授权。同时,基于该技术也开发了包括免疫肿瘤学、感染性疾病在内的多条管线,部分管线正处于临床前和临床试验阶段。
小结
随着新冠大流行逐渐进入尾声,多数企业将非病毒载体递送技术应用于肿瘤、罕见病等治疗领域,相应进展持续推动着非病毒载体递送技术的发展。目前,LNP递送技术和GalNAc递送技术已经得到临床验证,成功进入市场,后续我们期待更多的递送技术获得成功。
技术和专利是生物医药企业的核心竞争力,各企业在构建结构特异的递送系统时,一方面需要关注领域内其他人已经构筑的专利壁垒,以规避侵权的问题;另一方面,也建议对候选技术在领域中的位置进行系统化分析,明确候选技术的空间,为技术方案的设计提供思路,并构建相应的专利策略进行保护,从而为保持科学技术的市场竞争力提供保障。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
