用于保护医药用途的特殊的权利要求
在生物医药领域中,当新研发了一种全新的化合物或生物大分子,这些新的化合物或生物大分子对于某些疾病有预防和/或治疗的效果时;或者,意外地发现已知的化合物或生物大分子对于新适应症有预防和/或治疗的效果时,为了保护这样的发明,需要撰写合适的权利要求。然而,如果直接将权利要求撰写为“物质X在预防和/或治疗Y病中的应用”或者“使用物质X来预防和/或治疗Y病的方法”,那么该权利要求的主题就会属于“疾病的诊断或治疗”。但是并非所有的国家都接受“疾病的诊断或治疗”是可授予专利权的客体。如中国专利法第25条第1款第3项规定“疾病的诊断或治疗”不是能够授予专利权的对象。为了克服疾病的诊断或治疗方法不能被授权的障碍,1984年,瑞士联邦知识产权局创立了人们现在所称的“瑞士型(Swiss Type)”用途权利要求,并由欧洲专利局扩大上诉委员会(the EPO’s Enlarged Board of Appeal)以G05/83号决定的形式予以认可。我国也引进和应用了“瑞士型”用途权利要求,其典型撰写方式是:“物质X在制备用于诊断或治疗Y病的药物中的应用”。

在我国,采用“瑞士型”用途权利要求保护物质的医药用途。《审查指南2010》第十章4.5.2节“物质的医药用途权利要求”记载:“由于药品及其制备方法均可依法授予专利权,因此物质的医药用途发明以药品权利要求,或者例如“在制药中的应用”、“在制备治疗某病的药物中的应用”等等属于制药方法类型的用途权利要求申请专利,则不属于专利法第二十五条第一款第(三)项规定的情形。上述的属于治疗方法类型的用途权利要求可撰写成例如“化合物X作为制备治疗Y病药物的应用”或与此类似的形式”。
TiPLab磨杵君认为,从审查指南的上述记载的内容可以推知,“瑞士型”用途权利要求在我国被视为制药方法类型的权利要求,其本质上请求保护的是一种药物的制备方法。目前在申请和审查实践中,常见的用于限定瑞士型权利要求的技术特征可以总结为三大类型:第一种类型为治疗对象(如肿瘤、儿童白血病);第二种类型为给药方式(如口服、肌肉注射);第三种类型为给药方案(如每次服用剂量、服用频率)。上述的技术特征是否对“瑞士型”用途权利要求具有限定作用,影响着“瑞士型”用途权利要求的新颖性和创造性的判断。如,对于新颖性,《审查指南2010》第十章5.4节“化学产品用途发明的新颖性”记载:“对于涉及化学产品的医药用途发明,其新颖性审查应考虑以下方面:……(4)给药对象、给药方式、途径、用量以及时间间隔等与使用有关的特征是否对制药过程有限定作用。仅仅体现在用药过程中的区别特征不能使该用途具有新颖性”。对于创造性,《审查指南2010》第十章6.2节“化学产品用途发明的创造性”记载:“对新的化学产品,如果该用途不能从结构或组成相似的已知产品预见到,则这种新产品的用途发明有创造性;对于已知产品的用途发明,如果该新用途不能从产品本身的理化性质以及该产品的现有用途显而易见地得出或者预见到,而是利用了产品新发现的性质,并产生了预料不到的技术效果,则认为这种已知产品的用途发明有创造性”。
换句话说,无论是在判断新颖性还是创造性时,“瑞士型”用途权利要求中的技术特征是否真正对权利要求存在限定作用,需要落实到制药方法上,即是否会对药物本身及其制备方法产生影响。若是,则该技术特征才能被认为存在限定作用。然而,这些技术特征的限定与否判断的尺度究竟是怎样的?国知局和复审委为代表的行政系统与北京高级人民法院为代表的司法系统分别对上述判断的尺度持怎样的态度?这些问题在专利申请实践中还是困扰着大家。对此,TiPLab磨杵君将在后面的短文中通过讲述典型案例的小故事对上述问题进行初步的探讨。
此外,TiPLab磨杵君还想说明一下瑞士型权利要求在欧洲的命运。2007年12月13日《欧洲专利公约2000年修订案》生效,该公约修改案中的第54条(4)取代了1973年《欧洲专利公约》的第54条(5),新增的第54条(5)引用了EPO扩大上诉委员会于2010年2月19日做出第G02/08号决定,,直接采用医药用途限定产品:如果发现了已知药品的新用途,则可以直接以产品权利要求申请产品专利;同时,如果已知药品被发现可以用新的治疗方法(包括给药方案)治疗已知疾病,仍然可以申请产品专利。换句话说,EPO目前已经废止了瑞士型权利要求,而是使用医药用途限定的产品权利要求。医药用途(包括给药方案)也可以作为区别技术特征用以评价该产品权利要求的新颖性和创造性。可见瑞士型权利要求已经在欧洲完成了自己的历史使命。
最后,为了使大家在宏观上对医药用途发明所涉及的主要法律问题有一个大致的了解,TiPLab磨杵君对涉及复审程序的医药用途专利申请进行了统计。统计结果发现,位列前三的法律问题依次为:《专利法》第二十二条第三款、第二十六条第四款和第二十六条第三款。
表1 统计结果
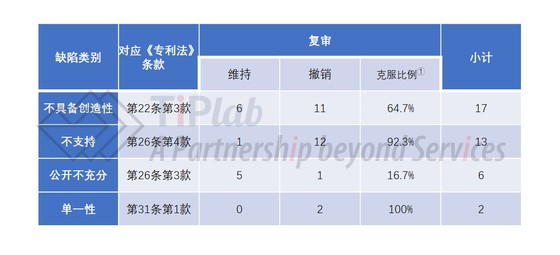
①“克服比例”的含义为涉及某一法律条款的所有复审案件中,最终复审决定为撤销驳回决定的案件占这些复审案件的百分比。
TiPLab磨杵君在此对上述的统计结果进行一些简单的说明,很多含有类似“医药用途”的表述的专利申请被驳回的主要问题并不真正在于医药用途发明本身,而是上述“物质X”本身的问题。如“物质X”是用通式概括的一类化合物,则经常会产生审查员认为通式涵盖的范围过大,得不到说明书支持的问题;或者,审查员认为“物质X”的制备方法没有交代清楚,产生了说明书公开不充分的问题;又或者,审查员认为含有这些通式的“马库什”权利要求存在不具备单一性的问题。排除这些干扰后,TiPLab磨杵君认为《专利法》第二十二条第三款涉及的创造性问题是目前瑞士型权利要求所面临的最重要的法律问题。医药用途发明的创造性问题如何判断和克服呢?TiPLab磨杵君将在后面的短文中通过小故事来进行初步讨论。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
