在医药领域,由于创新药的研发成本高昂,当保护药物活性成分的专利到期后,需要寻找有效的方法来延长产品的市场独占期,以延长产品的生命周期。
将药物活性成分制备为复方制剂,并且使得该复方制剂得到有效的专利保护,是医药领域重要的研发和销售策略,也是药品生命周期管理(PLM)的重要环节。在通过专利保护复方制剂的过程中,也有很多申请时机和申请策略值得我们重视和斟酌。
我们将以吉利德推出的复方制剂哈瓦尼(Harvoni®)为例,尝试探讨其中的时机和策略。
案例分析:Harvoni®
Harvoni®是一种处方药,其用于治疗成人伴有或不伴有肝硬化的慢性丙型肝炎(HEPC)基因1、4、5、6型感染。
Harvoni®作为吉利德销售的索非布韦(sofosbuvir)的第一种复方制剂,其活性成分包括索非布韦和雷迪帕韦(ledipasvir),每片Harvoni®中含有400mg索非布韦和90mg雷迪帕韦,患者每天只需口服一片Harvoni®。
Harvoni®于2014年10月在美国上市,2014年11月在欧洲上市。Harvoni®的销售额曾在2015年达到峰值138.6亿美元,目前依然属于吉利德最畅销的产品之一。

Harvoni®的专利保护
对于如此有价值的丙肝治疗产品,吉利德对Harvoni®的专利保护可以说是全方面、多层次的。
首先,吉利德对Harvoni®的活性成分索非布韦和雷迪帕韦分别进行了专利申请保护,尽管目前这些专利或专利申请命途多舛:
以索非布韦为例,其化合物的核心专利申请为WO2008/121634(PCT申请日为2008年3月26日),该PCT申请进入中国的申请为CN200880018024.2,该申请被驳回后于2015年就进入了复审程序,然而目前状态还是未决。
WO2010/135569(PCT申请日为2010年5月20日)涉及索非布韦的制备方法,该PCT申请进入中国的申请为CN201080032541.2,授权公告号为CN102459299B。
WO2005/003147(PCT申请日为2004年4月21日)涉及服用索非布韦后产生的代谢产物GS-461203和GS-331007,该PCT申请进入中国的申请为CN200480019148.4,授权公告号为CN100503628B。然而,ZL 200480019148.4于2018年5月30日因违反专利法第26条第3款说明书公开不充分等理由,被复审委宣告部分无效。
由此可见,保护活性成分可以至少从以下几个方面入手:
活性成分的化合物本身(包括可以描述其的马库什通式、晶型);
活性成分的衍生物(包括其盐、酯等衍生物以及其代谢产物等);和
活性成分的制备方法(包括其前体、中间体、副产物等)。
仅仅对药物的活性成分进行保护是比较薄弱的
同时,索非布韦在我国曲折的审查历史也从侧面证明了仅仅对药物的活性成分进行保护还是比较薄弱的。
一方面,索非布韦核心化合物专利申请即使马上授权,从申请日起算也历经十年之久,对后期研发的产品(例如,Harvoni®等以索非布韦为活性成分的复方制剂)保护的年数非常有限。
但同时,从另一个角度,重要的化合物核心专利一直处于悬而未决的状态的话,也可以在一定程度上起到震慑竞争对手的作用。因为大家都不期望投入了大量的资源研发后最终却得到侵犯他人专利权的沮丧成果。
另一方面,如果有关索非布韦的专利权难以获得预期的保护范围,就要求后期研发的产品具备更为直接和适当的专利权保护。
从组合物角度入手保护复方制剂
实际上,吉利德确实为Harvoni®提出了一系列的专利申请并在美国得到了很多授权,例如:
US 9511056B2(申请日 2014年5月16日)保护了一种减少病人丙肝病毒的方法,所述方法包括施用有效剂量的(1)如式I所示的化合物和(2)NS5B聚合酶抑制剂。
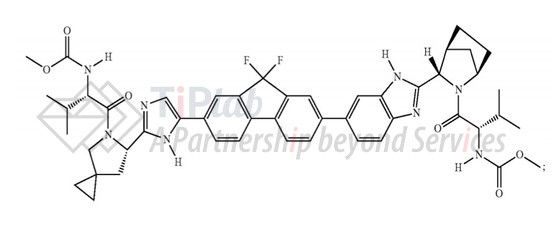
US 9393256B2(申请日2013年5月1日)保护了一种治疗人丙肝病毒感染的方法,所述方法包括施用(1)化合物10或其药学上可接受的盐和(2)化合物6或其药学上可接受的盐,其中所述方法不包括施用干扰素。
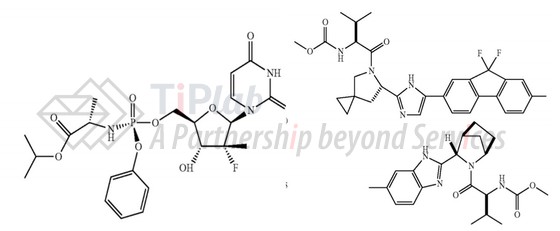
US 8889159B2(申请日2013年5月1日)请求保护一种药物组合物,其包含:a)约25%至约35%的具备结构I的晶型GS-7977和b)至少一种药学上可接受的盐,其中晶型GS-7977的XRPD2θ反射角(°)约为6.1和12.7。
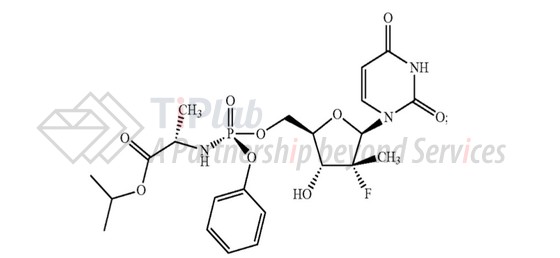
由此可见,保护复方制剂可以从组合物的角度入手,层层递进:
将不同种类的活性成分进行排列组合,得到含有不同含量、不同种类和/或组合的活性成分的组合物,使得该组合物作为该复方制剂的“活性成分”是对复方制剂产品最为直接的专利保护。
其他可以保护复方制剂的角度
此外,还可以进一步保护该复方制剂的“活性成分”的衍生物、代谢物、复方制剂的制药用途、治疗用途、前药、适应症、制备方法、中间体、制剂和剂型等。
这样做的好处有很多方面:
一方面,广泛的保护主题可以覆盖不同研发、商业化阶段产生的各项成果,为每一种具备可能的改进的产品和/或工艺都提供专利权角度的独占权,维护医药厂商的利益。
另一方面,Harvoni®至少已被记载在橙皮书中有关Harvoni®的专利列表中的16项专利所覆盖保护,而且可以预期的是,随着未来更多的专利申请(包括以上这些专利申请的分案、延续案、部分延续案等)在美国陆续授权,保护Harvoni®的专利数目还可能不断增加。
这时,各种竞争对手以各种目的希望无效这些专利的难度就会相应增大:
即使这些专利中的部分被不幸无效或部分无效,还有其他专利仍然能够发挥保护Harvoni®的作用,从而更好的保证吉利德对Harvoni®的独占地位。
专利保护与产品生命周期管理
按照本领域药品生命周期管理(PLM)的常规做法,通常会在研发的早期即以产品(一般以化合物通式限定权利要求)的形式对可能的药物活性成分提出专利申请。如果各项后续研发结果显示某种化合物可能具备良好的制药前景,则会选择在临床试验阶段对包括复方制剂等其他主题进行专利保护。
当然还需要特别指出的是,无论是复方制剂的专利保护还是PLM,都是相对比较复杂的事宜,需要通盘考虑某一特定产品的研发进度、商业策略和法律实践。
无论是针对例如吉利德的Harvoni®这样历史相对悠久、销量大、专利数量大的产品,还是针对销售体量小、专利申请数量相对较少的“小而美”的产品,都需要从早期开始重视专利申请策略,把握专利申请的时间节点,从而争取获得更有利的竞争优势。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
