Structure Therapeutics 专注于开发新型口服小分子疗法以治疗代谢性疾病(尤其是肥胖症)。
Structure在三维配体与靶蛋白结构可视化方面的洞见和能力,结合联合创始人及战略合作伙伴 Schrödinger 的计算化学能力,使其在高效、理性的药物设计方面具有显著竞争优势。
通过将对 G蛋白偶联受体(GPCRs)结构 的理解与基于物理原理的计算方法相结合来设计新型化合物,从而能够以较高的准确性预测分子与靶位点之间的结合亲和力。现已构建起一条广泛的口服小分子治疗药物研发管线,旨在克服生物制剂及多肽疗法所固有的局限性。
Aleniglipron(GSBR-1290) 是一种在研的口服小分子 GLP-1 受体激动剂,通过公司的structure-based drug discovery平台设计而成,aleniglipron 被设计为一种偏向性 GPCR 激动剂,在治疗剂量下选择性地激活 G 蛋白信号通路,而不激活 β-arrestin 信号通路,从而避免受体内化和脱敏。
除 aleniglipron 之外,Structure 还在开发下一代口服小分子药物,其中包括胰淀素受体激动剂,以及用于与 GLP-1R 激动剂或胰淀素受体激动剂联用的小分子,例如:靶向 GIPR 和 GCGR 的小分子候选药物。
目前已取得的研究数据持续为推进 aleniglipron 进入 III 期临床开发奠定坚实基础。公司已安排于 2026 年第二季度与 FDA 举行 B 类 II 期结束会议,以最终确定 III 期临床试验方案。该方案目前计划起始剂量为 2.5 mg,并评估高达 240 mg 的多个剂量。Structure Therapeutics 预计将于 2026 年下半年启动 III 期临床试验项目。
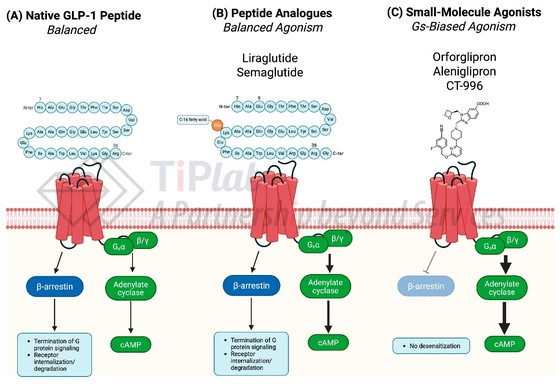
天然 GLP-1 及其肽类似物可同时激活GLP-1 受体的 Gs 和 β-arrestin 通路,从而产生平衡的激动作用,而小分子激动剂则优先激活 Gs 信号通路,β -arrestin 的募集量极少。
在小分子 GLP-1 受体激动剂中,aleniglipron 表现出近乎完全的 Gs 偏向性,β -arrestin 的结合可忽略不计;而 orforglipron(礼来)则表现出部分偏向性。
具体来说,aleniglipron 与 GLP-1 受体的非经典跨膜结构域(TM1、TM2 和 TM7)内的一个较深的正构空腔结合,而不与胞外结构域结合,因此具有 Gs 偏向性药理学特性,并减少 β-arrestin 介导的不良反应。
根据官方披露,Structure 的全资子公司 Gasherbrum 拥有 24 个专利族,涵盖主要候选产品 aleniglipron 及其类似物、固体制剂以及治疗与 GLP-1R 活性相关的疾病的方法的专利和专利申请,预计将在 2041 年至 2045 年之间到期。
- 多个专利家族围绕涵盖aleniglipron的通式化合物或其衍生物,比如:PCT/CN2021/075488;PCT/US2024/036066;PCT/CN2024/115894;PCT/CN2024/077096;PCT/US2024/061069。
- 专利家族PCT/CN2023/138803涉及aleniglipron的盐型和晶型。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
