在生物信息传递的中心法则中,核酸信息到生物大分子的转换是通过“RNA→蛋白质”的翻译过程完成的,tRNA作为翻译过程的重要参与者,帮助完成了将mRNA上的密码子解码成对应氨基酸的工作。
正是由于天然tRNA在核酸与氨基酸之间起到对应和转换的传递作用,因此工程化tRNA疗法不仅可以尝试解决由tRNA本身引发的问题,也可以尝试解决核酸密码子错误引起的相关问题。而在这其中,领域内目前研究较多的是通过tRNA疗法矫正mRNA密码子层面的错误,尤其是由无义突变导致的相关疾病。
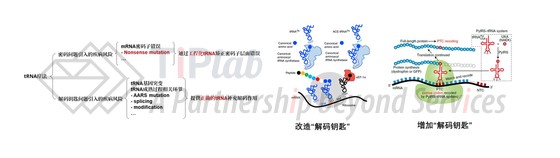
在本系列文章中,我们分别讨论了工程化tRNA在无义突变领域中两种主要的设计思路(“改造解码钥匙”和“增加解码钥匙”),这两类方法中的主要设计思路都是希望通过工程化改造tRNA的反义密码子区,使其能够结合在突变为终止密码子的相应位点,并最终在核糖体的作用下实现通读,从而实现完整多肽的合成。因此无论是第一类还是第二类设计思路,工程化tRNA都是重要的技术点。
反观tRNA疗法的发展史,在无义突变前正确密码子对应的tRNA的基础上,仅改造反义密码子区使其能够结合突变后的终止密码子(即不影响tRNA原本对应氨酰化的氨基酸类型),方案本身的可行性和有效性早已在上个世纪80年代的相关研究中已经得到基本验证。尽管工程化tRNA的基础技术已经比较成熟,但tRNA疗法领域一直没有停下探索的脚步,发展过程中也一直伴随着产生了许多新的发明。
在tRNA疗法的技术发展上,早期工程化tRNA主要尝试应用于不同的突变位置、疾病类型,逐渐慢慢开始入手优化tRNA的核酸修饰、结构序列,与此同时,国内的科学家们也紧跟tRNA疗法的开发热潮,在已经验证的理论基础上开拓了工程化tRNA新的研发设计方向(同时改造tRNA和AARS酶,即第二类“增加解码钥匙”),近几年也涌现了体内递送tRNA的相关研究…可以看到现阶段的tRNA疗法的设计,已经慢慢推进到提高效率优化方案细节的阶段。
从治疗潜力被挖掘到发展一度停滞,一直到2015年之后,领域内逐步成立了一批以tRNA疗法为研究方向的公司主体。其中2017年成立的专注CNS领域的Tevard Biosciences,公司官网显示已经获得了来自Whitehead Institute、The Johns Hopkins University等主体的相关技术IP许可,意味着tRNA疗法早已步入了前沿技术从高校科研院所向初创公司的转移转化阶段;同时在2023年初,Tevard也与上市公司Vertex Pharmaceuticals签订合作协议,合作开发治疗DMD的tRNA疗法。可见tRNA领域内无论是产品开发、技术的转移转化以及商业合作都比较活跃,在目前的竞争格局下,现阶段希望入局的玩家,对于产品开发过程中使用的技术和新产生的发明,建议在专利层面提前考虑潜在侵权风险和布局保护两个方面的问题。
由于工程化tRNA的原理成熟,同时早期使用的tRNA修饰类型与其他核酸药物修饰类型并无显著差异,意味着使用相关技术时,风险层面大概率不会再有非常宽泛的专利障碍,对于现阶段希望进入该领域的玩家来说,这无疑是能够甩开袖子大胆创新的有利前提。而选择不同的设计思路,需要关注不同的风险来源,例如涉及改造AARS酶的方案则需要关注单独来自改造酶的潜在风险。除此之外,由于工程化tRNA具备的通用性优势(即由相同无义突变引起的疾病,可能通过对应同一类型氨基酸的工程化tRNA进行治疗),因此我们仍旧建议在排查潜在侵权风险时,需要警惕来自同源氨基酸tRNA改造的相关保护(例如不限定具体适应症类型的专利障碍)。
另一方面在专利保护的角度,技术层面,“反义密码子区突变”的工程化tRNA大概率需要结合具体序列、相关基因突变/适应症或者tRNA修饰开展不同层次的保护;对于其他特殊改造的组分可以尝试单独保护、以组合的形式进行保护,比如“重构翻译系统”设计中的AARS酶变体、非天然氨基酸。
对于布局策略的实施,通常情况下,初创企业在早期有初步的技术开发思路时,就可以围绕领域内现有技术的情况,配合早期拟定的商业策略等,入手开展专利布局策略的规划,以便在早期合理的规划并辅助协调后续其他的资源投入成本。随着研发进程的推进,在后续开发过程中,围绕产品研发过程中遇到的特定技术问题,以及产生的具体发明,适应性调整布局策略的实施。通过布局策略的动态调整,真正实现专利保护跟随商业目标走,为产品的研发创新保驾护航。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
