本文中,我们将分别从开发和使用三种不同的主流环化技术:Group Ⅰ intron PIE、Group Ⅱ intron PIE和Clean PIE的企业Orna Therapeutics、环码生物以及科锐迈德讲起,对他们分别递交了哪些专利资产保护核心技术进行梳理。
MIT和Orna Therapeutics的专利保护
Orna Therapeutics基于Group Ⅰ intron PIE做了一些改进,其优化策略是通过同源臂和间隔序列的添加设计增加目标序列的长度。该公司的创始团队是来自麻省理工学院(MIT)的Daniel Anderson和Alexander Wesselhoeft,相关改进技术的专利权属于MIT,Daniel Anderson和Alexander Wesselhoeft也是其中的关键发明人。MIT在2019年递交了PCT专利申请(WO2019236673A1),该专利家族在主流国家以及一些经济较发达的国家和地区都有布局,在美国已有至少4件专利获得授权。
MIT的专利申请WO2019236673A1的权利要求1请求保护“一种用于制备环状RNA的载体,所述载体包含以下彼此可操作地连接并按以下顺序排列地元件:a. 5’同源臂,b. 3’Ⅰ组内含子片段,其包含3’剪切位点二核苷酸,c. 5’间隔子序列,d. 内部核糖体进入位点(IRES),e. 蛋白质编码区或非编码区,f. 3’间隔子序列,g. 5’Ⅰ组内含子片段,其包含5’剪接位点二核苷酸,和h. 3’同源臂,所述载体允许在真核细胞内产生能够翻译或具有生物活性的环状RNA。”
可以看出,MIT在权利要求中主要针对其核心技术优势同源臂和间隔子序列的添加进行了限定,针对其他特征,例如I型内含子的种类、IRES的来源及选择、同源臂的长度、间隔子的序列未做具体限定。这就意味着,这件专利申请可能阻止第三方基于该设计思路对IRES序列的序列做替换、使用不同来源的Ⅰ型内含子、或者对同源臂的长度做调整,换句话说,即使是使用与实施例中不同的Ⅰ型内含子、IRES种类、同源臂的长度和序列设计,也仍可能落入该权利要求的保护范围中。
随着对环状RNA领域的持续探索,Orna Therapeutics也在技术改进和应用上有进一步的专利布局。例如,其在通过增加duplex region或选择合适的内含子的置换位点优化PIE系统(WO2021236855A1和WO2022261490A2)、包含环状RNA和递送载体的药物组合物(WO2020237227A1)、包含环状RNA和特定通式的阳离子LNP的药物组合物(WO2021113777A3、WO2021226597A3),以及具有两个目标表达序列的环状RNA(WO2021189059A3)等方向都递交了一些专利申请。这些后续的专利保护能够为第三方进行核心技术优化或将核心技术应用至疾病治疗中设置障碍。
环码生物的专利保护
环码生物使用的是基于Group Ⅱ Intron PIE的技术,对比Group Ⅰ Intron PIE,环码生物的核心优势在于使用了Ⅱ型内含子,这样可以通过仅使用外显子上的内含子结合序列(IBS)减少残留的E1和E2序列的长度。还可以更进一步将目的基因的一部分序列视为IBS并突变相应内含子中的外显子结合序列(EBS),实现将E1和E2的序列长度缩短为0。
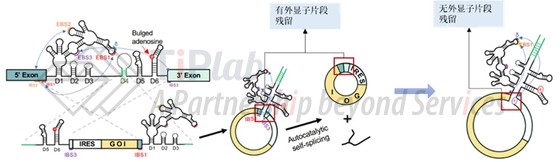
基于该技术优势,环码生物分别递交了中国专利申请(CN115404240A)和要求该中国专利申请优先权的PCT专利申请(WO2022247943A1)。
这两件申请在权利要求1中都请求保护“一种在体外具有自剪接活性的多核苷酸构建体,其从5’到3’包含以下可操作地连接的元件:(1)3’内含子片段;(2)外显子片段2(E2);(3)目标序列;(4)外显子片段1(E1);(5)5’内含子片段,其中5’内含子片段和3’内含子片段通过将 II 型内含子分割成两个片段获得,所述5’内含子片段在所述 II 型内含子中位于3’内含子片段的5’侧,所述E1为所述 II 型内含子的5’紧邻外显子片段,其长度≥0个核苷酸,所述E2为所述 II 型内含子的3’紧邻外显子片段,其长度≥0个核苷酸,所述目标序列为空,或为蛋白编码序列和/或非编码序列。”
在这两个专利申请中,实质仅限定了内含子的种类为 Ⅱ 型内含子和一些基本元件组成,这一范围涵盖了E1和E2序列为任意长度的情况。在从属权利要求中进一步限定了内含子进行分隔的domain,以及EBS的具体修饰等特征。也就是说,如果是基于Ⅱ型内含子制备环状RNA,在一些序列层面的优化(例如,内含子如何修饰)或者增加非编码区元件的设计(例如,加入间隔序列、翻译调控序列等)等很有可能还是会落入该申请的保护范围。
科锐迈德的专利保护
科锐迈德针对新开发Clean-PIE系统也有专利布局,Clean-PIE的优势集中在筛选合适的可以作为剪接位点的位置,通过将IRES区或编码区进行截断来设计核酶识别位点,从而无需引入E1和E2外源序列。科锐迈德还建立了一套剪接位点自动化筛选优化系统,针对不同序列计算出最佳的成环位点,并相应地设计截断的位置,用来提高环化效率。
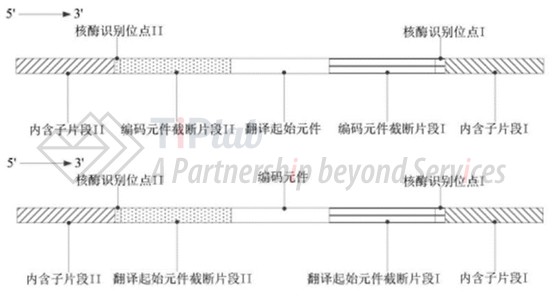
该公司针对Clean-PIE系统的设计思路,递交了两份专利申请(CN114438127A和CN114574483A),分别涉及将编码区和翻译起始元件(例如,IRES)截断的两个技术方向,这两件专利申请在最宽的权利要求中也仅对构建体的主要元件组成(包括编码区/翻译起始元件截断片段的核心设计)进行了描述,未对内含子的种类、翻译起始元件的种类、编码区中可以编码的目标多肽的类型等做更多限定。因此,这两件专利可能阻止他人通过截断IRES区或者编码区来设计剪接位点,从而避免引入外显子序列以降低免疫原性。
在后续的进一步的细化和改进方案的过程中,科锐迈德还针对翻译起始元件IRES的序列(WO2022116528A1)、筛选IRES的方法和筛选出来的IRES的序列(CN115966258A和US20230119715A1)、包含环状RNA分子的药物组合物(CN115804853A)等进行了专利保护。其中,上述专利申请中涉及的IRES序列可以应用于制备环状RNA的多种载体中,用于改善RNA分子的递送和表达的药物组合物设计也可能在未来应用于环状RNA的药物制备。相关专利申请都有可能帮助企业巩固未来在环状RNA领域的竞争优势。
从以上几个例子可以看出,不同企业基于自身的研发方向和技术优势都在积极进行专利布局,这体现在:首先在底层专利申请中会围绕这些核心技术优势进行保护,使专利保护的范围与实际的创新点相匹配。其次,从整体构建专利资产的角度,除了底层专利以外,企业也会配合后续研发中所产生的技术优化方案,或者更具体的产品形态以及用途进行专利申请,这些专利申请作为一个整体,帮助企业实现专利资产配置的灵活性和多样化,也能进一步巩固对于未来产业中可能使用的技术方案的保护力度。
在研发比较早期的领域,各个企业都有机会产生创新性很强的发明,通过合理的投入,创建与研发中创新程度相匹配的专利资产,能够有助于企业建立竞争优势。那么,处于类似环状RNA这样早期发展领域的初创企业在进行专利布局时重点是什么?还需要进一步关注和考虑哪些问题?在下一篇文章中我们将尝试针对这些问题进行总结和探讨。
