从靶向配体出发的创新主要体现在两个方向:其一,开发新的靶向配体;其二,将现有靶向配体应用于RDC领域。对于新的靶向配体,可单独对其进行专利保护;而对于已有配体的改进,则可对包含该配体的前体组合进行专利保护。下面将分别阐述这两种情况下,专利权利要求的设计思路及可能遇到的审查挑战。
靶向配体的专利保护
在RDC药物研发的早期阶段,企业可以对新开发的靶向配体构建通式,并进行单独的专利保护。在对通式的保护过程中,通常会遇到“支持问题”,其判断依据是,本领域技术人员是否可以合理预期,在通式所涵盖的范围中的所有等同替代方式都能具有相同的效果。
随着产品开发进入后期,商业化产品的特征逐渐清晰,企业可在结构通式基础上,针对靶向配体的关键结构细化专利保护范围。在构建了较为完善的靶向配体权利要求之后,企业还可以进一步扩展保护方向,保护包含靶向配体的前体结构,形成全方位的多层次保护。
以诺华开发的FAP-2286为例,其是一种与FAP结合的环状肽,可偶联放射性核素实现诊疗一体化,已开发出一款177Lu标记的靶向成纤维细胞活化蛋白(FAP)多肽偶联核素产品,目前处在I/II期临床阶段。
申请人首先递交了专利家族PCT/EP2020/069308(申请日2020年7月8日)对一类配体进行了单独的专利保护,并在从属权利要求中宽泛地限定该靶向配体能够与任意螯合剂和任意接头共价连接,涵盖了FAP-2286的结构组成。目前,该专利家族在中国已获得专利授权(公开号:CN114341158B),其权利要求1采用“马库什权利要求”方式,通过通式结构涵盖具有共同母核的可变取代基组合,保护了一类环状肽结构。
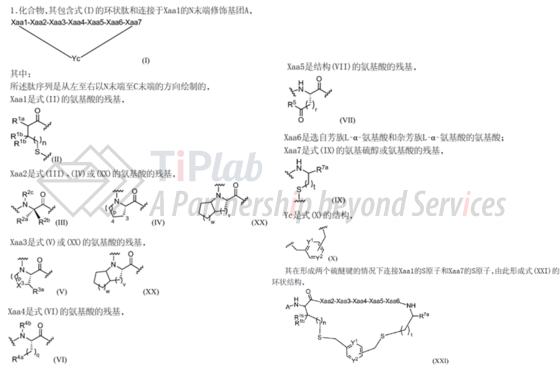
当商业化产品的特征逐渐明确时,可以考虑更为针对商业化产品的小范围专利,比如后续专利家族PCT/EP2022/050280(申请日2022年1月7日)围绕靶向配体做了进一步限定,同样未限定linker、螯合剂或核素类型,仍然涵盖FAP-2286的结构组成,这种保护方式能够有效阻止竞争者将本专利保护的一类配体应用于RDC领域。
在对于靶向配体单独进行专利保护时,由于靶向配体产生治疗效果的关键因素是结合能力。因此,在评估上述专利的授权前景时,主要关注的技术效果是靶向配体的靶向能力。同时,由于通式涵盖了较宽的保护范围,常常会遇到“支持性”问题。
比如,在CN114341158B的审查过程中,主要关注的焦点在于权利要求1所概括的较大的环肽范围是否都具有FAP活性——即是否得到说明书支持。
对于这类问题,申请人可以尝试从以下角度进行解释:证明说明书实施例与权利要求的涵盖范围存在“合理预期”。
具体而言,权利要求1所涵盖的化合物都含有相同的苯基二硫醚部分,并且按照取代基种类可以分为不同的类型。在实施例中,通过三种不同的测定方法,提供了80种配体的FAP结合活性,分别展开了通式中所列出的肽取代基(比如己基Hex、辛基Oct等)、保护基取代基(Abl)(比如戊基NH-脲、戊基-SO2等)和氨基酸取代基(Aaa)(比如4-吡啶基4Pya、氨基磺酰丁基H2NSO2-But、乙酰化高丝氨酸AC-Hse、乙酰化α-氨基己二酸AC-Aad等)的广泛组合。
此外,实施例中还列出数据说明了具有缀合的螯合剂的化合物与不含螯合剂但肽序列相似的化合物具有非常相似的活性。
通过对具有不同取代基的代表性化合物的活性测试结果,本领域技术人员可以合理地确定权利要求所有要求保护的化合物都具有FAP结合活性。
前体组合的专利保护
在RDC药物开发中,当申请人基于已有研究的配体开发产品时,可通过通式-限定关键技术特征-具体结构的递进式权利要求设计,构建多层次专利壁垒。
1.通式
基于靶向配体、连接子(linker)、螯合剂的组合逻辑,申请人可以尝试构建以通式结构为核心的平台式权利要求。在这种情况下,需要注意现有技术是否已公开类似组合逻辑,如果是,那么该宽泛权利要求的创造性可能存在较大的挑战。
在PCT/US2008/073375专利家族(公布文本WO2009026177A1,申请日2008年8月15日)中,申请人最初想要保护PSMA配体+linker+药物的概念。

然而对比文件US20070160617A1公开了一种PSMA抗体-药物缀合物,其中linker部分的结构通式为An-Ym-Zm-Xn-Wn,A与PSMA配体相连接,Y和Z为氨基酸,W与药物相连接,n为0或1,m为任意选自0-6的自然数。对比文件1公开了包含至少7个原子的linker,即公开了WO2009026177A1(申请文件)中linker的范围。同时公知常识已公开配体含义,配体为能够与受体特异性结合的蛋白,所以抗体满足配体的概念。
结合对比文件和公知常识,申请文件中的PSMA配体、linker和药物组合的技术特征均被公开,且并未说明特定的linker能起到意料不到的技术效果,因此该技术方案的效果是可预期的,也即缺乏创造性。
最后在相应进中国和进美国的授权专利中,保护范围限定到了具体结构的前体组合。
2.关键技术特征的进一步限定
基于前体组合的关键技术特征进一步限定保护范围,划分“小而精”的保护范围,通过限定关键技术特征以涵盖效果较优的一类结构,对申请人来说也十分有价值。
关键技术特征的确定在于明确前体组合中的改进点,基于此进一步限定保护范围。
胃泌素释放肽受体(GRPR)在常见人类癌症(例如前列腺癌和乳腺癌)中高密度表达。申请人基于已有研究的GRPR拮抗剂蛙皮素(bombesin,BN)类似物,将其应用于构建一个新的RDC,构建后的GRPR配体组合仍具有良好的GRPR亲和力和体内稳定性。在该技术方案中,关键技术特征在于使组合仍有较好效果的GRPR配体和linker。
PCT/US2013/061712专利家族(申请日2013年9月25日)中,申请人具体限定了靶向配体和linker的结构,对于螯合剂只进行了宽泛的限定(参见以下家族成员US9839703B2的权利要求1)。该保护范围涵盖了产品177Lu-NeoBOMB1的结构组成。

相应地,由于前体组合通常是基于现有技术的改进,因此常常会遇到创造性问题。也就是说,需要考虑现有技术是不是能给出改进技术特征的启示,以及改进后的技术效果是否能够基于现有技术合理预期。
在专利家族PCT/US2013/061712进入美国和欧洲的审查过程中,都遇到了相似的创造性问题。
对比文件1(Nock等人,DOI:10.1007/s00259-002-1040-x)公开了一种GRPR拮抗剂蛙皮素类似物(bombesin,BN),其肽链(P)结构为DPhe-Gln-Trp-Ala-Val-Gly-His-Leu,并且将其应用于构建RDC,能与锝99mTc稳定结合。
对比文件2(Heimbrook等人,J. Med. Chem. Vol 34, pages 2102-2107)公开了GRPR肽链(P)结构为Ac-His-Trp-Ala-Val-Gly-His,且公开了His末端具有NH-CH-CH[CH2-CH(CH3)2]2基团的GRPR配体可能有更强的GRPR拮抗剂活性。
审查员认为,申请文件的技术方案组合了上述对比文件,蛙皮素的N末端用NH-CH-CH[CH2-CH(CH3)2]2基团修饰,并且选择了已知linker,构建出一种新的RDC。现有技术给出了组合的启示。
然而,判断申请文件的技术方案是否是上述对比文件的简单组合,不能单单只看技术特征,还有一个关键因素,即,需要考虑组合所带来的优越的技术效果是什么,这样的技术效果是不是很容易预料到。
在RDC领域中,前体各部分之间的相互作用是非常复杂的,对于前体组合任意部分的替换都需要考虑到整体的效果。例如,配体稍加改动(比如缺失DPhe基团)可能会改变前体组合的体内药代动力学稳定性,替换成短肽(比如NH-CH-CH[CH2-CH(CH3)2]2)也可能会使得螯合剂的连接位置发生变化,同时linker的选择也会直接影响最终化合物的药代动力学特性(如靶向性、代谢稳定性)。也就是说,对于RDC领域而言,将另一个技术领域的现有研究应用到本领域后的效果是不经验证无法得知的。
同时,申请文件的实施例结果证实,与具有相似结构和组成的GRPR拮抗剂相比,申请文件的方案在给药4h后的肿瘤摄取率接近30%ID/g,在给药24h仍然高达25%ID/g,显著高于参考文献中GRPR拮抗剂的肿瘤摄取率2.01±0.34%ID/g和2.29±0.3%ID/g(Abd-Elgaliel WR 等人,Bioconjug Chem. 2008; 19:2040-48)。这样的数据表明,申请文件中方案的技术效果相比于现有研究有显著的“差距”,进一步说明了预料不到的技术效果。
由此可见,本领域技术人员即使结合多个对比文件,也难以合理预期权利要求1的前体组合能够达到上述预料不到的技术效果。
3.具体结构
对于效果特别优异、已验证临床优势的的产品,可以单独申请专利保护其具体的前体结构。这种保护范围相对来说较小,但更为稳定,可以灵活用于交易许可、药品专利有效期延长等方面。例如,PCT/EP2014/002808专利家族及其衍生专利还进一步保护了Pluvicto的具体前体结构(参见以下家族成员US10398791B2的权利要求1),该权利要求范围目前在中国、美国、欧洲等主要市场均已获得授权。

通过这种分层次保护体系,申请人可以设计由前体通式到具体结构的差异化专利保护,在确保核心专利稳定性的同时,构建难以绕过的专利壁垒。
基于靶向配体特点构建专利保护策略
综合上述讨论,在RDC领域,从靶向配体出发,可以依据不同的特点构建专利保护:
当靶向配体的创新程度比较高,与现有技术区别较大时,可以对靶向配体单独进行专利保护,并通过合理构建通式权利要求扩大保护范围。此时可能会遇到支持性问题,申请文件应提供有代表性的不同替代方案以支持大的保护范围。
当靶向配体是基于已有配体进行改进时,可以设计通式-限定关键技术特征-具体结构的差异化保护层次。此时可能会遇到创造性问题,申请文件可考虑针对该改进提供对比实验以体现权利要求保护方案的独特优势。
那么,围绕RDC产品,还可以从“制剂”的创新角度进一步构建专利壁垒,我们将在下一篇文章中继续介绍该角度的理想保护范围和技术优势。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
