Tiragolumab与PD-1抑制剂产生协同效应
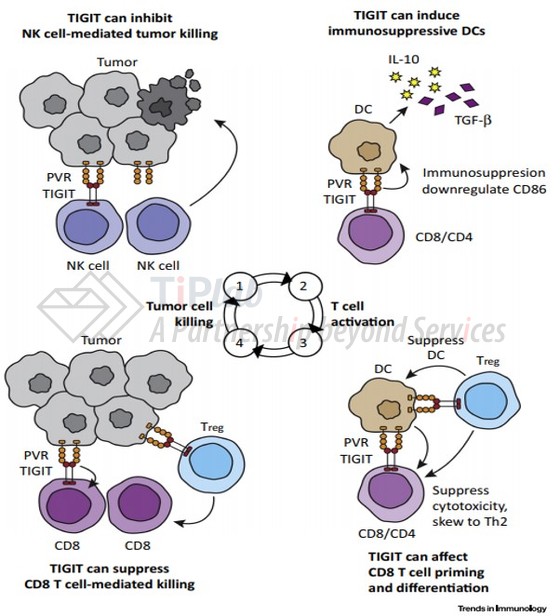
TIGIT是一种抑制性受体,在淋巴细胞中表达,比如:多种类型的T细胞(包括肿瘤浸润T细胞)和NK细胞上高表达。TIGIT通过与激活性受体CD226竞争和CD155(PVR)的结合,从而抑制淋巴细胞的激活,因此,当肿瘤表面高表达的CD155与NK和T细胞表面的TIGIT结合,它们对肿瘤细胞的杀伤作用就会被抑制。
通过与TIGIT结合,tiragolumab阻断了其与CD155的相互作用,且与PD-1抑制剂联用可能协同激活T细胞,增强NK细胞的抗肿瘤活性。
PD-1和TIGIT还在具有干细胞特征的记忆T细胞中有表达。因此,同时靶向PD-1和TIGIT通路,除了可以逆转T细胞耗竭以外,还可以增加具有干细胞特征的记忆T细胞的数目。从而产生更多的效应T细胞,达到更好的杀伤肿瘤的效果。
2020年的ASCO年会上,罗氏公布了tiragolumab与PD-L1抑制剂Tecentriq(atezolizumab)联用治疗非小细胞肺癌的二期临床试验的结果,取得了不错的疗效,且已经在2020年初启动3期临床试验。2020年6月,罗氏已经在中国递交了tiragolumab的临床试验申请。
Genentech的专利保护策略
对于tiragolumab这个候选产品来说,有两个重要的发明点需要递交相应的专利申请重点保护起来,一个是TIGIT抗体本身,另一个是抗TIGIT抗体和PD-1抑制剂联用。
那针对这两个发明点应该分别在什么时机以什么撰写方式递交专利申请能够最大限度地延长专利期限呢?
这里Genentech采用了一种比较有意思的策略:
简单地说,Genentech先开发了一些TIGIT抗体(不同于tiragolumab),并发现其与PD-1抑制剂联用效果不错,就分别针对抗体和联用这两个发明点递交了专利申请,之后开发了经优化的TIGIT抗体,也就是后来进行临床开发的tiragolumab,并递交了新的专利申请,我们大概梳理了一下时间线:
1)早在2009年,Genentech就递交了保护TIGIT抗体的PCT申请(PCT/US2009/039868),这个家族涉及了TIGIT抗体的多组序列,但并不涵盖tiragolumab;
2)2014年,Genentech递交了保护TIGIT抑制剂和PD-1通路结合拮抗剂联用的PCT申请(PCT/US2014/046896),从实施例或一些从属权利要求中限定的TIGIT抗体序列来看,使用的正是2009年递交的PCT/US2009/039868中披露过的序列;
3)2016年,Genentech又递交了涉及TIGIT抗体的PCT申请(PCT/US2016/053368),权利要求涵盖tiragolumab。
也就是说,Genentech从最早递交TIGIT抗体的专利申请到后来递交真正走上临床试验的TIGIT抗体的专利申请间隔了7年之久,这中间可能经历了一些波折,亦或是有意而为之,我们暂且不去纠结,接下来我们看看Genentech如何构建专利申请文件并实现延长生命周期的目的。
抗体家族—PCT/US2009/039868
Genentech的发明人在2008年分离获得了TIGIT,制备了TIGIT抗体以研究对信号传导的影响,并递交了PCT/US2009/039868,该家族中目前已经有不少专利获得了授权,授权专利最后都限定了TIGIT抗体的具体序列,主要涉及到两组抗体序列,以CN102057272B为例:
“1) 一种抗TIGIT抗体或其抗原结合片段,包含:含有SEQ ID NO :23所示的CDR1序列、 SEQ ID NO :24所示的CDR2序列和SEQ ID NO :25所示的CDR3序列的轻链;和含有SEQ ID NO :26所示的CDR1序列、SEQ ID NO :27所示的CDR2序列和SEQ ID NO :28所示的CDR3序列的重链。
5)一种抗TIGIT抗体或其抗原结合片段,包含:含有SEQ ID NO :31所示的CDR1序列、 SEQ ID NO :32所示的CDR2序列和SEQ ID NO :33所示的CDR3序列的轻链;和含有SEQ ID NO :34所示的CDR1序列、SEQ ID NO :35所示的CDR2序列和SEQ ID NO :36所示的CDR3序列的重链。”
在PCT/US2009/039868的说明书中,并没有提及任何TIGIT抗体与PD-1拮抗剂联用的内容,也不会对后来递交联用申请的新颖性和创造性造成影响。
宽泛的联用家族—PCT/US2014/046896
PCT/US2014/046896家族中有至少5个专利获得了授权,且授权的权利要求都相当宽泛。
我们以US10626174B2为例,US10626174B2的权利要求中一共有3个独立权利要求,使用不同的特征进行限定,发明点分别是PD-1通路结合拮抗剂和PVR拮抗剂用于治疗癌症、病毒感染或增强免疫响应:
“1. A method for treating or delaying progression of a cancer in an individual, the method comprising administering to the individual an effective amount of (i) a PD-L1 binding antagonist that inhibits the binding of PD-L1 to PD-1 and/or B7-1, a PD-1 binding antagonist that inhibits the binding of PD-1 to PD-L1 and/or PD-L2, or a PD-L2 binding antagonist that inhibits the binding of PD-L2 to PD-1 and (ii) an antagonist of TIGIT expression and/or activity.”
这些独立权利要求对于PD-1通路结合拮抗剂(包括PD-L1/PD-1/PD-L2结合拮抗剂)和TIGIT拮抗剂都属于功能性限定,对于使用任何PD-L1结合拮抗剂和TIGIT拮抗剂联用治疗癌症或病毒感染的竞争者至少到2034年之前都设立了一堵墙,可以说这个专利家族对于Genentech占领联用的市场有很大的优势。
我们再看PCT/US2014/046896的说明书,提供了大量的数据证明联用的效果和机理,其中描述TIGIT抗体的序列正是之前抗体家族中提及的序列,Genentech使用这些抗体获得了部分试验数据。
涵盖tiragolumab的专利家族—PCT/US2016/053368
PCT/US2016/053368家族中其中一个授权的US专利为US10047158B2,权利要求的写法比较中规中矩,其中最宽泛的权利要求1限定了结合TIGIT抗体的6个CDR序列,所以使用与tiragolumab同样的CDR序列但不同的FR序列也会落在权利要求的范围中。
联用方案的保护策略
针对联用的方案通常包括抗体药物本身的序列和联用方案两个发明点,在递交专利申请的过程中,通常是分别递交不同的专利家族以尽可能延长联用方案的专利保护期。
Genentech关于tiragolumab的专利申请策略提供了一个很好的范例,比如:不在早期的申请文件中披露之后可能进行开发的技术方案、一旦研发有新的发现就递交专利申请、提供充足的数据以支持尽可能宽泛的权利要求范围等,当然,这与研发企业的研发推进策略也有很大的关系,在确定保护策略的时候,应当通盘考虑研发推进速度、未来的计划和已经取得的结果合理规划。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
