REGN1979在1期临床试验中取得积极结果
REGN1979是一款抗CD3 × CD20的双特异性全人源IgG4抗体,由Regeneron公司开发。REGN1979能够同时结合T细胞表面抗原CD3和B细胞肿瘤细胞上的CD20,通过交联免疫细胞和肿瘤细胞,触发特异性的局部T细胞活化,从而对肿瘤细胞发起攻击。
REGN1979与罗氏的双特异性抗体mosunetuzumab展开了直接竞争。
根据Regeneron在2018年美国血液学会 (ASH)年会上公布的结果,5~40mg剂量REGN1979在治疗复发或难治性滤泡性淋巴瘤 (FL)患者的小型试验中达到100%的总缓解率 (ORR)和80%的完全缓解率 (CR)。虽然在滤泡性淋巴瘤一线治疗中取得高缓解率并不稀奇,不过100%的总缓解率仍然十分振奋人心,Regeneron计划于2019年开展临床2期研究,探索其作为一线疗法的潜力。

在治疗复发或难治性弥漫性大B细胞淋巴瘤 (DLBCL)方面也获得积极结果,接受剂量为18 mg~40 mg REGN1979治疗的总缓解率达到60% (10名患者中有2例完全缓解,4例部分缓解),Regeneron计划继续对DLBCL进行剂量递增试验。
早在2017年,FDA已经授予REGN1979治疗DLBCL的孤儿药资格。

此外,已证明REGN1979具有可接受的安全性和耐受性,没有观察到剂量限制性毒性和临床意义的神经毒性。
Regeneron还在探索REGN1979与其开发的Libtayo® (靶向PD-1的单抗)联用的治疗应用。
与我们之前介绍过的开发双特异性抗体的公司相比,Regeneron进入这个领域并不算很早,REGN1979的成功开发可能得益于Regeneron将其双特异性抗体平台技术与其已有的全人源抗体技术结合了起来。
Regeneron的双特异性抗体平台技术
为了获得异源二聚体,Regeneron在一条重链的Fc区引入突变来解决HC/HC的错配问题,并使用共同的轻链来解决LC/HC错配问题。这类双特异性抗体包含两个相同的轻链和两个不同的重链,从而形成异二聚体。
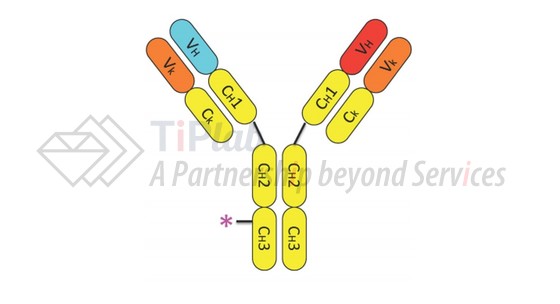
已有研究表明,在重链Fc区的CH3结构域引入氨基酸取代 (His435/Tyr436,称之为Fc*)可以消除与蛋白质A的结合能力,使用蛋白质A的选择性纯化可以获得Fc-Fc*双特异性产物。
保护此技术的代表性专利申请US12/823838和PCT/US2010/040028于同一天递交,并要求美国临时申请US61/220687的优先权,PCT/US2010/040028进入了全球包括EP、CN、US、JP等多个国家或地域。
对于重要的基础技术,除了在本土进行专利申请,申请人通常会使用PCT申请进入国家阶段的方式以获得在全球市场的保护。当然,进入的国家或区域与公司早期的商业策略密切相关。
基于此双特异性抗体构建策略,Regeneron设计了靶向CD3 × CD20的双特异性抗体,从而获得了REGN1979。REGN1979包含靶向CD20的重链、靶向CD3的重链以及靶向CD3的共同轻链,其中在靶向CD3的重链Fc区引入氨基酸取代。REGN1979由IgG4抗体构建得到,以降低Fc区的效应子功能。
Regeneron的VelocImmune小鼠平台
为了尽可能降低抗体的免疫原性,Regeneron对小鼠的部分免疫基因位点由相应的人免疫基因位点取代或“人源化”,以产生优化的全人源抗体,即VelocImmune小鼠平台。REGN1979正是由VelocImmune转基因小鼠平台生产获得。
Regeneron递交了多个涉及VelocImmune平台的专利申请,这些专利申请构成了阻挡竞争对手的技术壁垒。比如:
US6596541B2 (申请号US09/784859)主要涉及一种在分离的非人真核细胞中,使用同源或直系同源的人免疫球蛋白可变基因座以全部或部分替换内源免疫球蛋白可变区基因座的方法,并公开了具体的替换方法。
随着对VelocImmune平台技术的开发或改进,Regeneron以US6596541B2为母案,陆续递交多达19件衍生专利申请,部分已经获得授权,还有部分处于在审状态。
Regeneron还以US09/784859为优先权,递交了PCT国际申请—PCT/US2002/004500,并进入了EP、JP和DE等多个国家或地域。
可见,除了瞄准美国市场之外,Regeneron还将目光扩展至全球多个市场。
围绕REGN1979的专利申请
保护活性成分的专利家族
Regeneron围绕REGN1979也设计了合理的专利申请策略。比如:
PCT/US2013/060511专利家族涉及结合人CD3的抗体或同时结合人CD3和人CD20的双特异性抗原结合分子。
与PCT同一天递交的美国专利申请US14/031075已经获得授权 (US9657102B2),授权后的独立权利要求保护同时结合CD3和CD20的双特异性抗体。
US9657102B2的两个延续申请分别涉及结合人CD3的抗体或同时结合人CD3和CD20的双特异性抗原结合分子 (US20170320948A1)以及使用相关抗体治疗疾病的方法 (US20180215823A1)。
保护治疗方法的专利家族
除了上述提到涉及活性成分的专利家族之外,Regeneron还有一些涉及双特异性抗体治疗方法的专利家族。比如:
2015年递交的PCT/US2015/021322和PCT/US2015/061139专利家族分别涉及使用结合人CD20和人CD3的双特异性抗体抑制肿瘤生长 (比如B细胞肿瘤或CD20阳性肿瘤)的方法以及使用双特异性抗体治疗或改善B细胞肿瘤的方法 (公开了给药剂量方案),这两个专利家族涵盖了正在进行临床试验的适应症;
2016年递交的PCT/US2016/068003专利家族涉及使用特异性结合CD3 × CD20的双特异性抗体治疗或抑制患有急性淋巴细胞白血病的受试者中白血病肿瘤细胞生长的方法。
双特异性抗体的临床疗效值得期待
REGN1979的临床试验结果可能为双特异性抗体可以改善传统单抗的疗效提供依据,目前全球仍有多款双特异性抗体处于临床1期或2期研究阶段,期待这些双特异性抗体能够取得更多积极进展,并创造出新一代的重磅炸弹。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
