PMO改造的反义寡核苷酸药物—eteplirsen
Eteplirsen(商品名:EXONDYS 51®)是第一款获批的使用PMO改造的反义寡核苷酸,用于治疗Duchenne肌营养不良症(duchenne muscular dystrophy,DMD),适用于已确诊DMD基因突变且适合外显子51跳过的患者,根据患者用EXONDYS 51®治疗后观察到的骨骼肌中肌营养不良蛋白增加而获得FDA的加速批准。
DMD是由于基因缺陷使得肌肉细胞不能正常产生一种称为Dystrophin(肌营养不良蛋白)的蛋白质,从而引起全身性肌肉进行性退化。Eteplirsen通过与肌营养不良蛋白pre-mRNA的第51外显子结合,从而在mRNA加工过程中将该外显子排除在外,产生内部截短的肌营养不良蛋白并发挥作用。
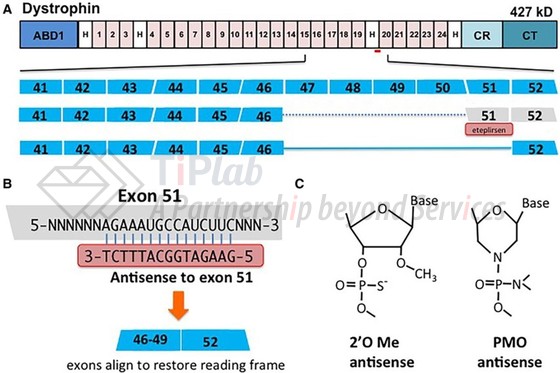
Eteplirsen的结构设计
Eteplirsen为磷酰二胺吗啉代寡核苷酸(phosphorodiamidate morpholino oligomer,PMO)结构的反义寡核苷酸,且5’端连接聚乙二醇的结构,长度为30个核苷酸,分子式为C364H569N177O122P30,通过静脉输注给药。
PMO以六元吗啉环代替天然DNA和RNA中的五元呋喃糖基环,每个吗啉环通过电中性的磷酰二胺基连接,而不是通过天然DNA和RNA中带负电的磷酸酯连接。每个磷酰二胺吗啉亚基均包含一种DNA中的杂环碱基(腺嘌呤、胞嘧啶、鸟嘌呤或胸腺嘧啶)。
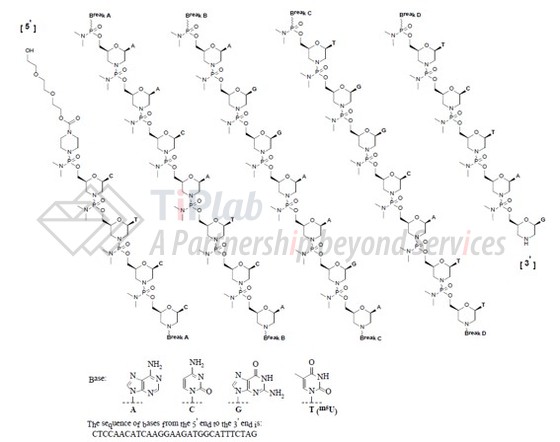
Eteplirsen相关的专利家族
PMO结构设计相关专利家族
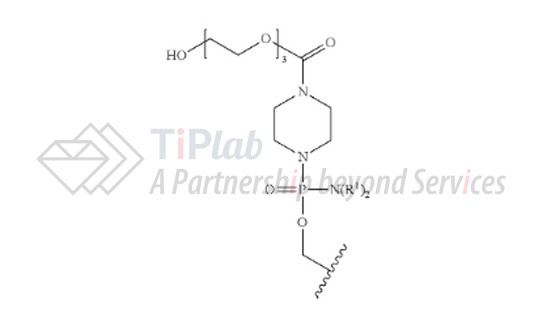
针对eteplirsen的PMO结构设计,Sarepta获得授权的美国专利US9416361B2的权利要求1保护通过含磷的亚基间键连接的8至40个吗啉代亚基的寡聚物,且限定了5’端吗啉代亚基包含下式的基团(每个R1独立地为C1-C6烷基),涵盖eteplirsen的结构设计。
US9416361B2的权利要求9和16均保护包含PMO结构的寡核苷酸的通式,限定了核苷酸的长度和两端的吗啉环结构,范围比较宽泛,其中权利要求16涵盖eteplirsen的结构设计。
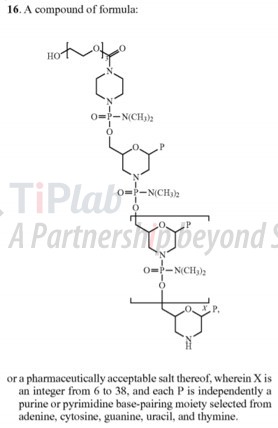
US10533174B2则保护一种药物组合物,包含寡聚物或结构通式,限定方式与US9416361B2类似,US9416361B2和US10533174B2都预计于2021年5月到期。
Eteplirsen活性成分专利—因PTE最晚至2029年到期
Sarepta从University of Western Australia (“UWA”)获得了涵盖eteplirsen活性成分专利的独占许可,包括:US9018368B2(涉及序列和结构)、US10781451B2(涉及序列和结构)、USRE47751E1(涉及医药用途)和USRE47769E1(涉及序列和注射剂)。
其中前三件美国专利的预计将于2025年到期,而USRE47769E1则因获得了专利期延长(PTE)有效期将至2029,这意味着,对于想开发eteplirsen仿制药的竞争者而言,来自序列或制剂方面的风险一直持续至2029年。
US9018368B2的权利要求1保护具有30个碱基的反义寡核苷酸,限定了核苷酸的碱基序列,且限定反义寡核苷酸是吗啉代反义寡核苷酸,并且其中反义寡核苷酸化学连接聚乙二醇链,涵盖eteplirsen的序列和结构特征。
“1. An antisense oligonucleotide of 30 bases comprising the base sequence CUCCAACAUC AAGGAAGAUGGCAUUUCUAG (SEQ ID NO: 181), in which the uracil bases are thymine bases, wherein the antisense oligonucleotide is a morpholino antisense oligonucleotide, and wherein the antisense oligonucleotide is chemically linked to a polyethylene glycol chain.”
US10781451B2的权利要求1同样限定了反义寡核苷酸的碱基序列,并限定反义寡核苷酸是吗啉代反义寡核苷酸,涵盖与SEQ ID NO: 181碱基序列相同的任何吗啉代反义寡核苷酸。
“1. An antisense oligonucleotide of 30 bases comprising the base sequence CUCCAACAUC AAGGAAGAUG GCAUUUCUAG (SEQ ID NO: 181), in which the uracil bases are thymine bases, wherein the antisense oligonucleotide is a morpholino antisense oligonucleotide.”
再颁专利USRE47751E1,主要涉及使用包含SEQ ID NO: 181的反义寡核苷酸或其可注射溶液的医药用途,包括:诱导肌营养不良蛋白基因中外显子51的跳跃;纠正肌营养不良蛋白缺陷基因;恢复或增加功能性肌营养不良蛋白产生;治疗与肌营养不良蛋白缺陷基因相关的肌营养不良症等用途。
USRE47769E1主要涉及两个发明点:特定序列的反义寡核苷酸和包含特定序列反义寡核苷酸的注射剂。对于反义寡核苷酸,限定序列为SEQ ID NO: 181;对于注射剂,除了限定序列为SEQ ID NO: 181,还限定反义寡核苷酸化学连接至聚乙二醇,并限定了不同的给药方式。USRE47769E1获得了长达1315天的专利期延长,有效期至2029,这意味着,对于想开发eteplirsen仿制药的竞争者而言,来自序列或制剂剂方面的风险一直持续至2029年。
Eteplirsen给药方案专利—将保护期延长至2034年
Sarepta依靠给药方案专利将eteplirsen在美国的保护期延长至2034年,这进一步给仿制药开发者设置了障碍,包括:US9506058B2、US10364431B2和US10337003B2。
其中,US9506058B2和US10364431B2都是主要涉及静脉内给予eteplirsen或其药物组合物每周一次且持续给药超过120周用于治疗DMD、恢复肌营养不良蛋白产生、减少DMD患者肺功能丧失或行走能力损失等用途,涵盖FDA批准的给药剂量。
US10337003B2保护一种在具有适合于外显子51跳跃的DMD基因突变的人类受试者中治疗DMD的方案,包括使用包含eteplirsen和磷酸盐缓冲液的组合物,并限定eteplirsen的给药剂量是约30 mg/kg至约50 mg/kg,FDA批准的eteplirsen制剂也是一个磷酸盐缓冲液,因此,US10337003B2也涵盖已获批的给药方案。
围绕eteplirsen的专利保护设下的障碍
Sarepta通过自己递交或外部的独占许可为eteplirsen构建起了专利壁垒,并还通过专利期延长的方式进一步延续专利障碍。
以上文讨论的专利情况来看,从2016年eteplirsen获得首次批准,活性成分的专利保护最长至2029年,给药方案的专利保护一直可以延续至2034年,Sarepta有较长时间的独占权利,给仿制药上市也增加了不小的难度。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
