全球首款获批上市的MET抑制剂
Tepotinib(特泊替尼,商品名:Tepmetko)由EMD Serono(Merck KGaA制药部门)研发及推广,它是全球首款获批上市的口服c-MET抑制剂,用于治疗不可切除、MET外显子14跳跃突变的晚期或复发性非小细胞肺癌患者。
MET原癌基因编码一个受体酪氨酸激酶,并与其配体肝细胞生长因子(HGF)结合,通过RAS-RAF和磷酸肌醇3-激酶(PI3K)途径诱导下游信号传导。MET外显子14跳跃突变删除了MET近膜结构域,直接导致了MET信号的异常,而异常的MET信号可通过增加细胞增殖、存活、侵袭和转移来驱动肿瘤的生长。
Tepotinib通过与ATP竞争,以阻断其靶标的磷酸转移酶活性,从而治疗MET外显子14跳跃突变的NSCLC患者。

Tepotinib的活性成分专利
早在2006年,Merck KGaA递交了涉及Met激酶抑制剂的哒嗪酮衍生物的PCT申请(PCT/EP2006/010668)。该PCT申请要求保护的化合物主要为被酰胺基苄基取代的哒嗪酮衍生物。
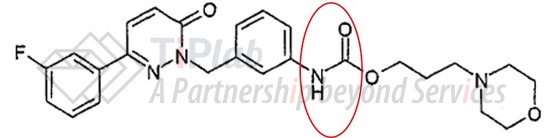
Tepotinib的结构,在上述PCT申请结构的基础上进行了较大的改构,将酰胺(上述红圈)替换为嘧啶,从公开的tepotinib/c-Met共晶结构上看,嘧啶外侧裸露的N原子或与c-Met形成氢键,有学者认为该氢键或能增加tepotinib的活性。
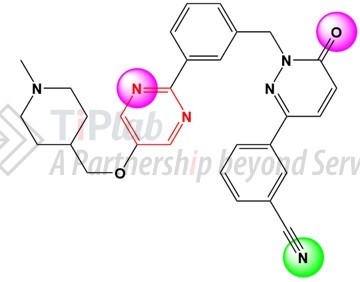
在2007年,Merck KGaA递交了1篇德国申请,并以该申请为优先权基础,再次递交了2篇涉及tepotinib活性成分的PCT申请,分别涵盖tepotinib的游离碱(PCT/EP2008/003473)及其盐(PCT/EP2008/005508)。

PCT/EP2008/003473
2008年4月,Merk KGaA首先递交了涉及tepotinib游离碱的PCT申请(PCT/EP2008/003473)。该申请进入了US、CN、JP、EP等多个国家和地区,并获得了不同范围的权利。
PCT/EP2008/003473(简称‘473申请)说明书中披露了313个化合物,其中A257为tepotinib的游离碱形式;此外,实施例部分还涉及优选化合物在细胞水平的Met激酶抑制活性,且A257的IC50值为1nM-1μM。
可见,‘473申请对A257的制备合成及体外药效均进行了实验,对该申请后续进入各个国家阶段拿到稳定权利提供了有利支持。
‘473申请进入美国国家阶段的授权专利为US8580781B2,权利要求1保护一种通式I的化合物或其药学上可接受的溶剂化物、盐、互变异构体或立体异构体,并对取代基进行了马库什限定。

以US8580781B2为母案,其授权分案US8921357B2获得了更大的保护范围,该分案同样保护了一种通式I化合物,其与母案的区别在于:R2为含1-4个N、O和/或S原子的不饱和、饱和或芳香族6元杂环,范围十分宽泛,几乎涵盖了所有常见的6元杂环,对以tepotinib为微改构对象的制药企业设立了较大的障碍。
此外,US8580781B2的分案还包括US8927540B2(涉及医药用途)和US9284300B2(药物组合物)。
‘473申请也进入了肺癌的主流市场中国,在中国的授权专利为CN101743241B,其授权范围相对于美国授权专利来说,缩小了很多,独立权利要求1仅涉及12个具体化合物及其可药用的盐或互变异构体。

PCT/EP2008/005508
继tepotinib游离碱申请递交3个月后,Merk KGaA依据自己的研发进度,再次递交了涉及tepotinib药物上可接受盐的PCT申请(PCT/EP2008/005508),并要求前述同一德国申请的优先权。
PCT/EP2008/005508(简称‘508申请)进入美国国家阶段的授权专利为US8329692B2,其独立权利要求1保护了14种具体的盐,涵盖FDA获批的tepotinib的盐(tepotinib hydrochloride hydrate)。

‘508申请进入中国国家阶段的授权专利为CN101687857B,其独立权利要求1与US8329692B2的授权范围相同,此外,其余从属权利要求还涉及该14种含盐化合物用于治疗Met激酶信号转导的疾病。
同样,‘508申请说明书,记载了14种具体盐化合物的制备及结构表征数据,以及14种具体盐化合物在细胞水平和酶水平上的Met激酶抑制活性,且IC50均低于100nM,可见,该14种具体盐化合物均能得到说明书的支持。
依据目前中国专利的审查实践,在发明具备新颖性、创造性、实用性的前提下,若进一步体现说明书对权利要求的支持,后续该授权的权利要求在面对竞争对手的无效时,也将相对稳定。
小分子药物中,盐型专利的重要性
目前上市的小分子药物,大部分都是相应活性成分的盐型,因为,化合物的盐可在某种程度上改善药物本身的溶解性,提高药物的生物利用度。
从活性化合物出发,筛选生物活性更优的化合物盐型,通常看作是二次创新,因此,多数上市小分子药物,会在游离化合物申请之后递交相应化合物的优势盐型,作为后续上市产品的主要活性成分。
此次,Merk KGaA在tepotinib活性成分专利布局上,依据同一篇优先权申请,同时递交了游离碱及盐型的专利申请,可能是根据其研发进度,在确定先导化合物和优势盐型后,立刻提出了专利申请,最大限度的降低市场风险。
盐型化合物作为重要的活性成分专利,通常在实质审查阶段需与审查员进行多次争辩,其障碍多源自在先提交的游离化合物专利和公司披露的相关信息过多,从而,导致盐型申请缺乏新颖性或难以证明创造性,因此,制药企业在布局盐型专利时需要重点考虑其布局时机。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
