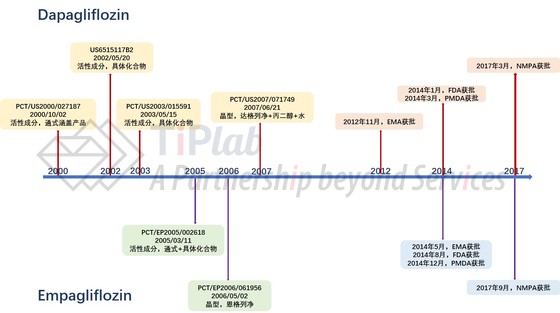
达格列净与恩格列净先后获批
Empagliflozin(恩格列净,Jardiance®),由勃林格殷格翰发现,于2011年与礼来达成合作联合开发的糖尿病药物。该药为SGLT2抑制剂家族中的一员,这类药物独立于胰岛素发挥作用。
SGLT2是一种转运蛋白,参与肾脏近端肾小管的葡萄糖重吸收。SGLT2抑制剂药物主要通过抑制表达于肾脏的SGLT2,减少肾脏对葡萄糖的重吸收,增加尿液中葡萄糖的排泄,实现降低血糖水平。
早在恩格列净进入临床之前,Dapagliflozin(达格列净,Farxiga®)便以首款SGLT2抑制剂的角色进入临床。
在制药领域,从最初的立项到后续产品上市及上市后监控,整个过程花费资金最多的便是新靶点的验证和临床试验。达格列净进入临床,一定程度上已经验证了SGLT2靶点作用于糖尿病是可行的。
基于糖尿病的市场占有率可逾百亿,在巨大的市场需求推动下,于2005年勃林格殷格翰携带恩格列净正式加入了SGLT2抑制剂行列,并于2014年5月获得欧洲药物管理局(EMA)批准上市,之后依此获批进入美国、日本、中国市场。
规避侵权风险,构筑专利资产
专利作为利益之源,是销售额的重要保证。在制药领域,基于首创优势分子进行结构修饰时,首先需要注意的问题就是规避原研专利的侵权风险,待后续筛选出全新的优势结构后,构筑自己的专利壁垒维护自身权益,提前保障后续市场的独占地位。
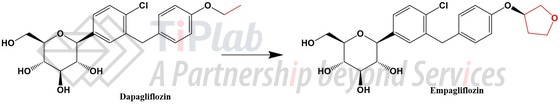
基于达格列净与恩格列净,从结构式来看,改动非常小,仅仅将达格列净右侧苯环上的乙基调整为四氢呋喃。
深入分析原研活性成分专利,提前规避侵权风险
早在2000年10月,BMS便开始布局SGLT2抑制剂靶点,递交了涉及活性成分的PCT申请(PCT/US2000/027187)。
该PCT申请进入中国国家阶段的授权专利为CN1284793C,该专利独立权利要求1涉及一种通式化合物,涵盖达格列净,但该家族实施例中并无达格列净的具体制备实验,也未对其结构进行表征。
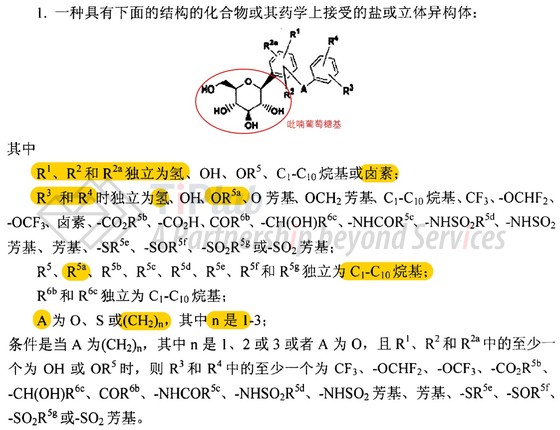
因此,在PCT/US2000/027187之后,BMS又递交了涉及达格列净具体结构的PCT申请(PCT/US2003/015591)。该PCT申请的目的十分明确,主要保护达格列净及其中间体,并在发明详述部分对其制备方法和结构进行了详细描述。
以上便是仅涉及达格列净活性成分结构的主要家族,在进行风险规避时,需详细分析其权利要求书和说明书的内容,以使新设计的结构不落入说明书中出现的结构和权利要求中。
从两份申请说明书涉及的结构中可以看出,吡喃葡萄糖基以及苯环是不能改动的,据此可推测该部分应当作为母核,对生物活性可能具有较大影响,为了更有说服力也可进行活性实验进行验证。
初步确定母核后,改构的重点大家通常会放在取代基上,结合实施例,分析原研结构取代基特点,改变取代基中必要的原子或片段,以达到规避侵权风险的目的。
达格列净活性成分专利实施例中涉及的结构,取代基主要围绕链状烷烃、卤素、醚、羧基、芳基等。该专利中取代基涉及的种类非常少,这也增加了以达格列净为基础,制药企业进行改构并成功规避侵权风险的几率。
此外,在初步确定新分子后,依据该分子的活性数据,再基于降低毒性、改善化合物血浆稳定性、化合物水溶性、血脑屏障通透性、降低hERG、代谢稳定性等方面进行针对性改构,以获得各方面实验数据较好的优势化合物。
确定优势化合物,构建专利资产
2005年,勃林格殷格翰递交了涉及恩格列净活性成分的PCT申请(PCT/EP2005/002618),该申请进入中国国家阶段的授权专利为CN103467423B。
CN103467423B的独立权利要求1同样涉及一种通式化合物2c,其通式结构与BMS的CN1284793C专利中的通式非常相似。为体现结构的不同,勃林格殷格翰对R3进行了定义,R3选自四氢呋喃-3-基氧基。
可以看出,在BMS结构基础上,勃林格殷格翰将原来的链状烷烃、卤素、醚等基团修改为四氢呋喃-3-基氧基,其它部分均保留了达格列净结构的特征。

以CN103467423B为母案,又先后递交了同样涉及恩格列净的分案CN103450129B、CN103435581B,分别从不同层次的范围出发,以更小通式和精准结构的形式,更加稳固的保护了活性成分。
优势化合物筛选与侵权风险规避并行
优势化合物的确定是新药研发的关键环节,专利作为保障市场独占地位核心资产,是打击竞争对手的有利武器,也是给予竞争对手启示的高风险点。
依据原研结构进行修饰时,需深入分析原研活性成分专利,必要时需要考虑原研公司为保护产品管线递交的化合物外围专利,提前规避侵权风险,待后续筛选出全新的优势结构后,及时构筑自己的专利壁垒维护自身权益,提前保障后续市场的独占地位。
