Cyramza®的横空出世
Cyramza®是礼来于2014年推出的一款癌症治疗药物,其活性成份为ramucirumab。Ramucirumab是一种重组人单克隆抗体,最早由ImClone研制,并随着ImClone被礼来收购而被持续开发,预期很快将进入重磅炸弹俱乐部。Ramucirumab通过结合VEGFR2(KDR/Flk-1)胞外结构域来阻止VEGF与其受体的相互作用,从而抑制血管生成。临床前研究显示ramucirumab与VEGFR2的亲和力高于其天然配体VEGF-A。2014年,FDA相继批准ramucirumab作为单一疗法或与紫杉醇联合使用治疗转移性胃或胃食管 (GE) 连接腺癌,与多西他赛联合使用治疗晚期非小细胞肺癌 (NSCLC) 。2015年4月24日,FDA批准ramucirumab与FOLFIRI (亚叶酸,氟尿嘧啶,和伊立替康) 联合应用来治疗晚期结肠直肠癌。
血管生成抑制剂已被批准用于治疗多种癌症和一些眼科疾病,包括原位和转移性实体瘤。临床使用的血管生成抑制剂主要分为两类:
1.酪氨酸激酶抑制剂 (TKIs) ,即抑制受体酪氨酸激酶 (RTK) 活性的化学小分子,例如sunitinib (舒尼替尼) 和sorafenib (索拉非尼) ;
2.蛋白质生物制剂,包括阻断血管内皮生长因子A (VEGF-A) 的单克隆抗体 (mAb) —bevacizumab (贝伐单抗) 和结合VEGF,VEGF-B和胎盘生长因子 (PlGF) 的重组融合蛋白—ziv-aflibercept等。
Ramucirumab作为一种新的生物制剂,受到了越来越多的关注。
在各种血管生成抑制剂中,结合VEGFR2的ramucirumab为何能继贝伐单抗后成为备受瞩目的品种呢?原因之一是VEGFR2通常在肿瘤血管中过表达并与肿瘤细胞转移相关,因此通过阻断VEGFR2信号通路能够直接抑制肿瘤的生长和扩散。现存用于临床治疗的血管生成抑制剂大多数为抗VEGF抗体,而只有少数药物直接作用于VEGFR2。所以,ramucirumab这个品种有其较独特的竞争切入点。
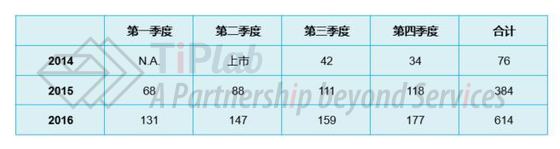
我们尝试在表1中总结了Cyramza®自2014年上市以来的销售情况,可以看到其销量保持稳中有升,增长主要来自于胃癌高发国家,例如日本。然而,迫于来自其它抗肿瘤药物 (例如,罗氏的Avastin、BMS的Opdivo和Merck的Keytruda等) 的竞争压力,2016年Cyramza®在美国的销售额略有下降。
从“潜力股”变身为“重磅实力派”
说到ramucirumab的开发过程,还有点小曲折。最初,ImClone合成了噬菌体展示来源的小鼠/人嵌合IgG1mAb cP1C11(IMC-1C11),并针对该抗体进行了肝转移性结直肠癌的I期临床试验,然而,事情一度没了下文。原来,ImClone对IMC-1C11进行了改造,从而获得了针对人VEGFR2的全人单克隆抗体 (编号为IMC-1121B,即今天的ramucirumab) ,并递交了专利申请PCT/US03/06459来保护这一经改进的抗体。研究显示,IMC-1121B的Fab和IgG形式对VEGFR2的亲和力相对于亲本分子分别高出36倍和4倍,并显著增强了该抗体抑制VEGF与人VEGFR2相互作用的能力。从临床前结果来看,该药确实具备一定的潜力。
2008年10月6日,礼来宣布以每股70美元,或总价65亿美元现金成功收购了ImClone。该报价比2008年7月30日ImClone的股价溢价51%。礼来的收购行为可谓诚意满满,因为此前一直与ImClone合作紧密的BMS曾两次向ImClone示好,并提出收购方案,不过都因出价不高被ImClone果断拒绝了。虽然礼来斥重金将ImClone收至麾下后,其股价一度下跌了7%,不过此次收购使得礼来成为了全球领先的肿瘤生物制药企业。礼来不仅获得了Erbitux这一肿瘤靶向的重磅药,还获得了三个有潜力的肿瘤靶向临床在研药物,其中就包括有IMC-1121B。当时正在进行该药针对转移性黑色素瘤、肾、肝、卵巢和前列腺癌的临床II期研究,针对转移性乳腺癌处于临床III期实验中,而针对胃癌的III期临床实验将在2009年开始。被收购后,ramucirumab由礼来负责继续开发并凭借良好的临床表现于2014年上市,由此成功变身为重磅实力派。
目前仍在进行的ramucirumab相关临床实验项目由礼来主导,实验项目主要涉及ramucirumab与化疗药物 (顺铂、多西他赛) 或抗体药 (抗PD-1抗体、抗PD-L1抗体、抗EGFR抗体) 联用治疗实体肿瘤 (肝癌、肾癌、尿路上皮癌、头颈部鳞状细胞癌等) ,并且有三个项目已进入临床三期阶段,预计会在未来几年得到批准。
重要的药物品种总是会以迅雷不及掩耳之势吸引各路人马围观并跃跃欲试。据报道,科伦药业最近公开了重组抗VEGFR2全人源单克隆抗体注射液的注册受理公告,该药是国内首个ramucirumab的生物类似药,由于该药针对的适应症转移性胃或胃食管连接腺癌、非小细胞肺癌和结肠直肠癌均为中国的高发的肿瘤,并且ramucirumab尚未进入中国市场,预计该药上市后将会具有不错的市场表现。
可见,一方面,原研药企业努力通过精心策划的专利布局来最大化专利的保护作用并保持竞争优势;另一方面,仿制药企业也试图规避原研药的专利保护并在一定范围内争取自己获得一部分专利权,从而在与旗鼓相当的对手 (例如,其它仿制药企业) 的竞争中脱颖而出。无论如何,对于双方而言,充分了解并利用专利保护策略都非常重要。
编织专利的网
礼来之所以斥重金收购ImClone,考察的核心当然首先在于ImClone管线上的品种是什么,潜在销量如何,在竞争中有何独特优势以及凭借什么取得或持续保持竞争优势,而ImClone围绕重要品种构建的专利保护网就像一道护身符将竞争对手甩在身后,使他们只能远观不可亵玩。那么,ImClone编织的这张专利之网到底是什么样子呢?
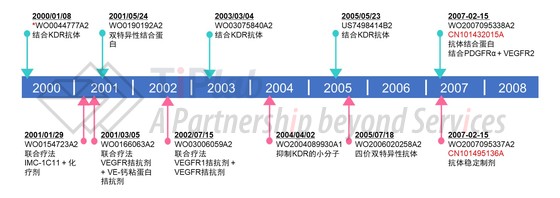
下图显示了ImClone针对ramucirumab提交的部分专利申请。整体来看,ImClone递交的专利申请虽然数量不是很多,但其针对可能被突破的各个“薄弱环节”分别进行有层次、有侧重的保护,使得规避起来非常困难。从2000年起,ImClone先是针对抗VEGFR2抗体及经改进的其各个变体提出了专利申请,并随后针对该抗体的制剂组合物、该抗体与其它药物的联合用药等进行了保护。
另外,我们都清楚,即使是对于药品这么特殊的商品,消费者(例如,开具处方的医生)在意的并不是产品特征本身,而是这个产品带来的益处。从生产厂家的角度考虑,除了希望排除“一模一样的仿品”外,还希望能够排除针对同样市场需求、带来同样益处的其它产品,这些产品也许结构不同、颜色不同、包装不同、味道不同,但只要带来了类似的益处并且没有不能容忍的缺陷,就一定会带来竞争压力。因此,在验证了VEGFR2作为药物靶标的重要性后,ImClone并没有止步于开发针对VEGFR2的抗体,而是同时研发了能够提供相同或相似益处的小分子化合物,并对于具有类似功效的小分子物质进行了专利保护,从而初步形成了一张专利保护网。
从不同类型技术分支的专利申请数量来看,核心专利数量相对较少,对于抗体变体和联合疗法专利布局数量较多,这些专利获得授权后不会同时过期,因此在一定程度上将延迟因专利过期带来的竞争压力,从而争取时间获得其他竞争优势。
此外,从核心专利申请的情况也可看出,专利保护应该是与研发结果紧密结合的过程,而非一锤定音的一次性决定,因为某项技术是否重要、是否应该公开、是否值得投入都是随着我们对技术前景越来越清晰的了解而逐渐变化的。这从ramucirumab的例子中可见一斑:
起初ImClone针对ramucirumab改造前的小鼠/人嵌合抗体 (IMC-1C11) 申请了专利PCT/US2000/002180 (WO0044777A2) ,但由于种种原因被撤回,没有得到授权。不过ImClone对抗体进行亲和力改造后合成了新的全人源抗体,在该新抗体的研发之始,ImClone就提交了PCT专利申请PCT/US2003/006459 (WO03075840A2) 。随后,PCT/US2003/006459进入美国国家阶段,获得授权的专利号为US7498414 (’414专利) ,该专利保护特异性结合VEGFR2的全人单克隆抗体 (即为ramucirumab) ,涵盖了不同的抗体类型。此外,ImClone还基于’414专利进一步在美国提交了分案申请,授权专利号为US8057791,并在其中保护了具有特定序列的抗VEGFR2抗体用于治疗肿瘤的方法。此后,ImClone开始了针对ramucirumab进行的临床实验。作为Cyramza®上市销售后,为了保持其市场竞争优势,礼来还基于’414专利向FDA提出了专利期延长申请。随后FDA于2016年4月批准了其请求,因此’414专利的保护期限被延长1059天直至2026年1月31日。值得一提的是,PCT/US2003/006459并没有进入中国国家阶段。
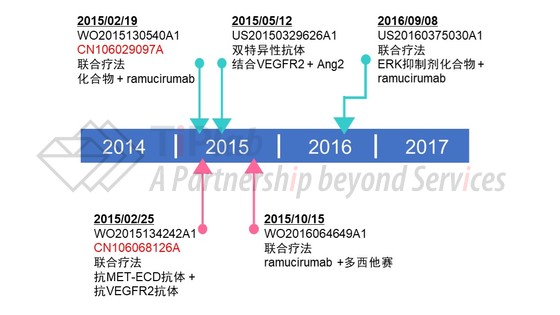
如上文所述,在ImClone时期,针对ramucirumab进行的专利布局已经比较全面,而礼来后期又在ImClone的专利网络基础上进行了拓展,进一步针对联合疗法和抗体变体进行了保护,并就联合疗法在中国递交了相关专利申请 (公开号为CN106029097A和CN106068126A),为以后进入中国市场做了相应准备,这两件专利申请目前仍然在审。下图简单介绍了礼来围绕ramucirumab提交的部分专利申请。
从上述分析来看,礼来及ImClone都围绕ramucirumab进行了积极的专利布局,仍希望进入这一领域的企业需要考虑自己的技术方案是否会落在这些 (以及其它)相关专利的保护范围内。此外,也应考虑在某个或某些方向 (效果、制剂稳定性、毒副作用等)上进行效果显著的改进,并通过合理的专利保护来武装自己,从而构筑属于自身的竞争壁垒。
无论是先行者还是后来者,都能够通过清楚地了解现有技术状况和现有权利的分布而看清机会与风险,之后才有可能基于客观事实做出理性判断。进也好、退也罢,都应该抛开一厢情愿的侥幸,也避免人云亦云的盲目,真正在权衡过利弊以后再进行决策。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
