有望成为第一款治疗黑色素瘤的肿瘤疫苗
M-Vax是一种治疗性肿瘤疫苗 (Therapeutic cancer vaccine),由自体黑色素瘤细胞经半抗原二硝基苯基 (Dinitrophenyl,DNP)修饰而成,DNP可以刺激基于T细胞的免疫应答和迟发型超敏反应 (Delayed-type hypersensitivity,DTH)。治疗方式为多次皮内注射M-Vax与免疫佐剂Bacille Calmette–Guerin的混合物。目前,M-Vax尚在美国进行III期临床研究,未获得FDA的批准。
治疗性肿瘤疫苗的常见形式有蛋白/多肽疫苗、细胞疫苗 (包括肿瘤细胞和树突细胞)和基因疫苗 (包括DNA和RNA等),之前讲过的治疗前列腺癌的肿瘤疫苗普列威® (Provenge®)属于树突细胞疫苗,而M-Vax则属于肿瘤细胞疫苗。
在一项使用M-Vax治疗黑色素瘤晚期患者的III期临床试验中,214位患者的5年生存率由手术的20%~25%提高至44%。
M-Vax由Avax Technologies进行开发,早在1999年,FDA就授予M-Vax为孤儿药。2001年,因涉及美国工厂的制造违规行为,FDA停止了M-Vax的两项关键性III期临床试验。Avax于2002年重新提交了新的IND (Investigational New Drug Application)申请,目前正在进行IV期黑色素瘤的III期临床试验。M-Vax已经于2005年10月在瑞士批准用于治疗III和IV期黑色素瘤。
David Berd首先开发了M-Vax
最初,来自美国费城的托马斯杰斐逊大学 (Thomas Jefferson University)的David Berd等人基于其自体细胞疫苗平台技术 (AC Vaccine)开发了M-Vax。
随后,Avax从托马斯杰斐逊大学获得了AC Vaccine的许可并继续进行M-Vax的开发。2004年,David Berd作为首席医疗官加入Avax公司,主要负责自体疫苗管线的开发。Berd博士在自体疫苗临床试验和产品开发方面拥有丰富的经验,他的加入极大推动了相关产品的开发进程。
活性成分专利
早在上世纪90年代初,Berd就发现半抗原化的自体肿瘤细胞可以诱导迟发型超敏反应,从而治疗转移性黑色素瘤,Berd为此递交了专利申请并获得了授权 (US5290551A),权利要求1保护:
“A vaccine useful for the treatment of melanoma comprising irradiated autologous melanoma cells conjugated to a hapten, said hapten selected from the group consisting of dinitrophenyl, trinitrophenyl, and N-iodoacetyl-N’-5 sulfonic 1-naphtyl ethylene diamine; and mixed with an immunological adjuvant, wherein said immunological adjuvant is Bacille Calmette-Guerin”
US5290551A保护用于治疗黑色素瘤的肿瘤疫苗,保护与半抗原缀合的经辐照的自体黑素瘤细胞,并与免疫佐剂Bacille Calmette-Guerin混合使用,于1994年就获得了授权,保护的正是M-Vax的活性成分,已经到期。
治疗方法专利
接着,Berd获得了US5290551A的部分延续案US7585512B1,保护使用经半抗原修饰的自体肿瘤细胞和佐剂来治疗肿瘤的方法,没有限定具体的肿瘤类型,保护范围较为宽泛。
除此之外,Berd还分别对具体的适应症进行了保护,比如:对使用经半抗原修饰的自体卵巢癌细胞和自体结肠癌细胞来治疗卵巢癌和结肠癌的方法进行了专利保护 (US6333028B1和US7560103B2)。
不过,这些治疗方法专利均已到期。
给药方案专利
Berd发现在首次施用肿瘤疫苗之前进行环磷酰胺预处理可以增强肿瘤疫苗的疗效,并获得了保护这一给药方案的相关专利 (US6458369B1),并没有限定肿瘤疫苗的类型,将于2019年到期。
随着临床研究的进一步开展,Berd作为发明人还递交了保护具体给药方案 (包括具体剂量和周期)的专利申请并获得了授权 (US7297330B2),获得了832天的专利期调整,将于2023年到期。
制剂专利
作为一种细胞产品,肿瘤疫苗的稳定储存对于实现其治疗效果也十分关键,Berd发现一定浓度的人血清白蛋白组合物可以更好的稳定半抗原化的肿瘤疫苗,并获得了保护半抗原化肿瘤细胞稳定制剂的相关专利 (US6248585B1),不过因未缴纳年费该专利权已经终止。
制备方法专利
Berd还发现肿瘤细胞不需要进行辐照这一处理同样可以防止其施用后在人体内的生长,从而简化了肿瘤疫苗的制备过程,并获得了专利保护 (US6403104B1),将于2020年到期。
Avax开发了一种新的疫苗储存技术
Avax获得了这一技术许可后,开发了一种将疫苗通过分装和冷冻以在其使用前保存数个月的技术,这将有助于其进行更大规模的临床试验和商业化应用。不过,Avax为此获得的专利US8435784B2却因为未及时缴纳年费而导致专利权终止。
Avax还发展了治疗肺癌的疫苗—LVax,并递交了一些专利申请,不过由于Berd等人在先前递交的专利申请影响了其在后申请的新颖性和非显而易见性,这些专利最后都放弃了。
可能是由于M-Vax早在20年以前就已经被开发出来,所以保护M-Vax的专利们或已到期,或接近到期。不过,M-Vax作为一种生物制品以及孤儿药,在其获批后可以获得为期12年的BLA独占期和为期7年的孤儿药独占期,这为阻止竞争对手提供了另一种保护。不过,更重要的是,Avax应当不断发展改进或新的产品来加强公司的壁垒。
未来个性化肿瘤疫苗将成为趋势
不同于抗体药物,肿瘤疫苗类药物属于一种细胞产品,虽然研发起步与抗体相当,但迟迟未能成为一种主流的治疗癌症的方法,可能基于以下几种原因:
其一,与传统疗法相比,大部分肿瘤疫苗未能显示出出人意料的效果,这可能有多方面的原因造成,比如:鉴定肿瘤特异性抗原较难,目前许多肿瘤抗原在正常细胞中也有表达,免疫原性较弱,而且个体间的肿瘤抗原存在差异;
其二,肿瘤疫苗不容易实现快速和大规模制备,目前Provenge®以及M-Vax这两款已经验证疗效的肿瘤疫苗都是采用自体肿瘤细胞进行制备,制备过程繁琐且不易获取足够数量的细胞。
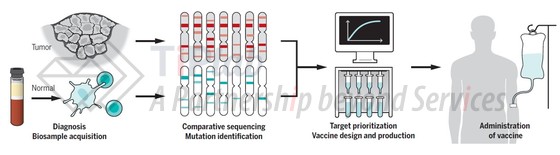
随着基因测序等技术的发展,个性化肿瘤疫苗将成为未来的发展方向,定制个性化肿瘤疫苗的过程包括:
取出患者的肿瘤组织,通过全基因组测序检测肿瘤细胞中存在的基因突变;
筛选出能够引起免疫反应的突变靶点并制备出具有独特表位 (即为所谓的neoantigen)的疫苗;
制备好的疫苗可以单独或与其他治疗方式 (比如:检查点抑制剂)联合使用。
最近,个性化肿瘤疫苗已经掀起了新一轮的研发和投资热潮,比如,Moderna Therapeutics是一家致力于个性化mRNA肿瘤疫苗开发的公司,已经与Merck达成合作探索肿瘤疫苗与检查点抑制剂组合疗法的应用。2018年5月,Merck宣布扩大与Moderna的合作,并投资1.25亿美元,共同进行个体化mRNA KRAS肿瘤疫苗的开发。
个性化肿瘤疫苗已经在临床试验中取得了一些进展,不过也存在一些挑战,包括:突变基因的准确检测、给药方案的优化设计 (比如:佐剂选择和肿瘤微环境的调节)、个性化疫苗快速生产和交付的能力等。随着大数据和云计算等技术的发展,将会极大推动个性化疫苗的实现。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
