罗沙司他中国率先上市
上周,2019年诺贝尔生理学或医学奖被授予William G. Kaelin, Jr.、Sir Peter J. Ratcliffe和Gregg L. Semenza 三位科学家,以表彰他们在细胞如何感知和适应氧浓度变化方面做出的贡献。
低氧诱导因子(HIF)是感应氧浓度变化的关键分子,由两种不同的DNA结合蛋白(HIFα和HIFβ)组成。HIF在细胞中积聚会激活下游多个基因(如促红细胞生成素EPO和血管内皮生长因子VEGF)的表达,因此HIF是贫血、肿瘤等多种疾病的潜在靶点。
脯氨酰羟化酶(PHD)能在不同氧含量下调节HIFα的活性和稳定性:常氧环境下,HIFα被PHD修饰,从而被降解;缺氧环境下,HIFα没有被修饰,不会被降解。而低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI)能抑制PHD的催化活性,在体内模拟缺氧环境,增加EPO的分泌,促进红细胞生成。
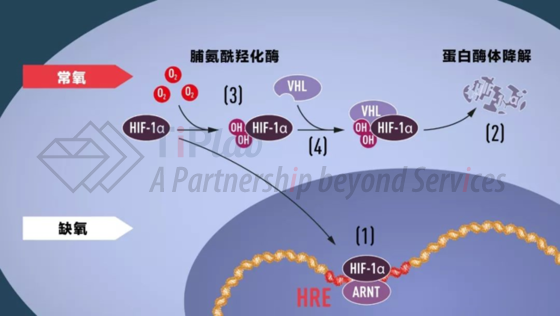
基于这一突破性的发现,全球首款HIF- PHI——罗沙司他(商品名:爱瑞卓®,通用名:roxadustat,研发代码:FG-4592)于2018年12月18日,经中国国家药品监督管理局(NMPA)通过优先审评审批程序批准上市,用于治疗正在接受透析治疗的患者因慢性肾脏病(CKD)引起的贫血。值得一提的是,中国是第一个批准罗沙司他的国家。
长期以来,EPO药物是肾性贫血的主要治疗药物。与EPO药物相比,罗沙司他的使用频率类似(2~3次/周),但罗沙司他为口服制剂,在依从性上具有巨大优势。
2019年8月,罗沙司他适应症范围扩大,获批用于非透析依赖性CKD患者的贫血治疗。
在中国所进行的治疗透析依赖(DD-CKD)和非透析依赖(NDD-CKD)的慢性肾病患者贫血状况的两项III期临床试验结果均达到了主要有效终点。在CKD患者的多个亚群中,罗沙司他能够维持EPO水平处于或接近正常生理范围,进而增加红细胞数量,同时不受炎症状态影响,也可避免静脉补铁。
同年9月,罗沙司他在日本获批上市,用于治疗透析慢性肾病患者的贫血,商品名为Evrenzo。
罗沙司他最初由珐博进(FibroGen)研发,2013年FibroGen和阿斯利康就罗沙司他在全球范围内的临床研发和商业化推广达成战略合作。同时,FibroGen也在与日本安斯泰来合作,合作进行罗沙司他在包括欧洲、中东和南非在内的等地区的开发。
罗沙司他活性成分
获批上市的罗沙司他胶囊有20 mg和50 mg两种规格,活性成分为N-(4-羟基-1-甲基-苯氧基异喹啉-3-羰基)甘氨酸,分子式为C19H16N2O5,分子量为352.3407。化学式如下:
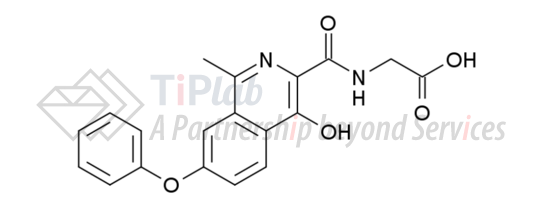
围绕罗沙司他的专利申请
活性成分专利家族
在罗沙司他的研发进程中,FibroGen首先递交了多项活性成分专利申请对其进行保护。
2004年6月4日,FibroGen递交了PCT申请PCT/US2004/017773,其进入中国国家阶段的专利申请为CN 200480015559.6,该申请被驳回目前处于失效状态。以CN 200480015559.6为母案,FibroGen又递交了4个分案申请,三个已被授权。其中,授权分案CN102977015B涉及保护了涵盖罗沙司他结构的通式。另一授权分案CN102977016B则对罗沙司他的结构进行了单独保护。
可以看到,关于罗沙司他活性成分专利的有效期已过大半。
晶型专利家族
2013年7月15日,以三个美国临时申请为基础,FibroGen同时递交了涉及化合物晶型的美国专利申请US2013/942443、中国专利申请CN 201310302481.7和PCT专利申请PCT/US2013/050539。
PCT/US2013/050539进入日本国家阶段的授权专利为JP6491093B2。
US2013/942443
US2013/942443及其衍生的延续申请主要涉及从衍射特征峰、特性晶型比例、制备方法等角度对化合物晶型进行限定。
US2013/942443已获得授权,公告号为US9115085B2,权利要求1涉及包括罗沙司他晶体形态A的药物组合物,具体如下:

,用3个衍射峰表征参数限定形态A。
在US9115085B2的基础上,FibroGen递交了一系列延续案申请,如2015年7月申请获得授权的US 9617218B2,权利要求1没有限定具体的衍射峰位置,仅限定了化合物A中晶型A的比例:

2017年3月递交的US9617218B2的授权延续案US10118897B2在权利要求中涉及罗沙司他晶体形态A的制备过程。
2018年10月,FibroGen又递交了US10118897B2的延续申请US 2019/0276408A1,权利要求1涉及通过将罗沙司他化合物和乙酸接触得到罗沙司他的结晶化合物,其中至少95%的结晶化合物A是形态A。
CN 201310302481.7
我们再把目光转向国内,CN 201310302481.7和衍生的分案主要包括特定晶型的药物组合物、其治疗用途和化合物衍生物的晶型等专利类型。
CN 201310302481.7已获得授权——CN103539735B,权利要求1保护一种包含罗沙司他晶体和药用赋形剂的药物组合物,用9个X-射线衍射峰以及差示扫描量热(DSC)表征形态A: 
CN103539735B的其它独立权利要求还分别涉及了所述药物组合物在制备治疗、预处理或延缓受HIF介导的病症、受EPO介导的病症,以及贫血症的药物中的用途。
此外,分案申请CN 201710546643.X的权利要求1涉及包含罗沙司他形态A的药物组合物,采用XPRD图谱的9个衍射峰限定了形态A的晶型。目前处于实质审查阶段。
在中国目前的审查实践中,对于采用X射线衍射图限定的化合物晶型,如果权利要求仅记载XRPD图谱的一个或少数几个衍射峰,所述技术领域的技术人员难以确定其表征的晶体就是请求人实际制得的晶体,会有权利要求得不到说明书支持的风险。
我们发现,FibroGen递交的不同晶型专利中,对于药物晶型的撰写方式,或采用多个衍射峰进行限定,或使用少数衍射特征峰结合其它技术特征进行限定,诸如:化合物晶型中形态A的比例、差示扫描量热等特征。
CN103539735B的其它分案还涉及治疗用途或化合物衍生物的晶型等:
比如,分案CN107501177B的权利要求1涉及罗沙司他形态A的晶体在制造药物中的用途,采用XPRD图谱的6个衍射峰限定了形态A的晶型:

分案申请CN201710546619.6的多个独立权利要求分别涉及不同化合物衍生物的多种晶型,包括罗沙司他及其盐。目前也处于实质审查阶段。
FibroGen构建了相当复杂的化合物晶型专利家族,可见,晶型专利对于保护罗沙司他产品或阻止竞争对手起到关键作用。
制剂专利家族
2014年6月5日,FibroGen递交了涉及罗沙司他药物制剂的PCT专利申请PCT/US2014/041021,其进入中国国家阶段的专利申请公布号为CN105377242A,权利要求涉及一种药物制剂,包含罗沙司他活性成分、药学上可接受的赋形剂和有效量的光稳定剂,以及少于约0.2% w/w的活性成分光降解产物。
CN105377242A的从属权利要求们分别对活性成分的含量、赋形剂的种类、光稳定剂的种类或含量以及药物制剂的剂型等做了进一步限定。目前处于实质审查阶段。
结语
伴随罗沙司他的研发过程,FibroGen在中国及世界范围内布局了广泛而交错的专利网络,特别对于晶型专利家族:分别涉及到了核心化合物的主要晶型、治疗用途、制备方法以及衍生物的晶型等,并且针对不同国家制定了差异化的撰写策略,可以说是小分子晶型专利撰写方法的经典案例了,这些为FibroGen之后布局全球市场打下了坚实了基础。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
