雄激素受体抑制剂Xtandi®
Xtandi®(通用名:enzalutamide,恩杂鲁胺)是一种口服雄激素受体(androgens receptor,AR)抑制剂,用于治疗转移性去势抵抗性前列腺癌(mCRPC)和非转移性去势抵抗性前列腺癌(nmCRPC)。
前列腺癌是常见的癌症之一,是导致全球男性死亡的第二大主要病因,仅次于肺癌。
通常,前列腺癌是由于雄性激素(最主要的形式是睾酮)过度表达导致的。因此,目前临床上针对前列腺癌的主要治疗方法是降低患者体内的雄性激素水平,包括外科手术去势和/或雄激素剥夺疗法(ADT)。雄激素受体(AR)是前列腺癌发生发展的重要因素,即使在去势抵抗性前列腺癌(CRPC)阶段,AR途径信号的激活仍然起着重要作用,其可能的机制有受体基因的扩增或过表达、基因突变、结构性受体改变及剪接变异体等。
Xtandi®能够选择性抑制雄激素受体(AR)、阻断AR途径信号转导,从而降低雄性激素水平。
2012年8月,FDA首次批准Medivation公司(后被辉瑞收购)与安斯泰来公司(Astellas,Inc.)联合开发的Xtandi®用于治疗已接受过多西他赛化疗的转移性去势抵抗性前列腺癌(mCRPC).该药上市后即成为重磅炸弹级产品,2015年、2016年的销售额均超过20亿美元。
2018年7月,FDA批准了Xtandi®扩大适应症的申请,用于治疗去势抵抗性前列腺癌(CRPC),这意味着Xtandi®成为首个也是唯一一个可以同时治疗转移性去势抵抗性前列腺癌(mCRPC)和非转移性去势抵抗性前列腺癌(nmCRPC)的口服药物。
2018年9月,欧洲药品管理局(EMA)批准了Xtandi®用于治疗高风险非转移性去势抵抗性前列腺癌(nmCRPC),进一步增加了该药的适用群体。
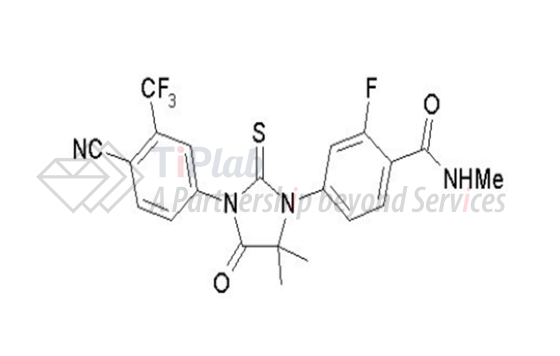
Xtandi活性成分
Xtandi®有效成分为恩杂鲁胺(enzalutamide). Enzalutamide 的分子式为C21H16F4N4O2S,化学名:4-[3-[4-氰基-3-(三氟甲基)苯基]-5,5-二甲基-4-氧代-2-硫酮-1-咪唑烷基]-2-氟-N-甲基苯甲酰胺,分子量为464.44 Dalton.化学结构如下
Xtandi制剂
FDA批准的Xtandi®制剂为40 mg的胶囊,推荐剂量为每日160 mg,分2次口服。辅料包含叔丁基羟基茴香醚、丁羟甲苯、脱水山梨糖醇、纯水、二氧化钛、甘油、明胶等无活性的成分。
围绕Xtandi的专利申请
活性成分专利家族
2006年3月,加利福尼亚大学递交了涉及活性成分的PCT国际专利申请(PCT/US2006/011417),要求了3个优先权。
2006年5月,加利福尼亚大学递交了涉及活性成分的US7709517B2美国专利申请 (授权公告号:US7709517B2),同时要求了4个美国临时申请的优先权,其中3个优先权文件与PCT/US2006/011417的优先权文件一致。权利要求涉及下列通式的化合物及化合物具有的显著的拮抗雄激素受体的活性。要求保护的化合物范围涵盖enzalutamide.
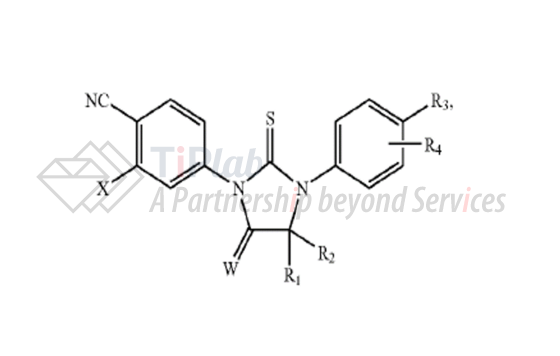
以US7709517B2为母案,2010年2月,加利福尼亚大学递交了涉及活性成分的分案申请(授权公告号:US8183274B2),权利要求涉及使用有效剂量的特定化合物治疗前列腺癌的方法,涵盖enzalutamide治疗前列腺癌的方法。
2012年4月,加利福尼亚大学还获得了延续案US9126941B2,权利要求涉及使用有效剂量的化合物治疗癌症的方法,要求保护的化合物范围涵盖enzalutamide.同年,Medivation公司从加利福尼亚大学获得开发enzalutamide的知识产权许可。
PCT/US2006/11417进入了包括EP、JP、CN等多个国家或地区,其中进入中国国家阶段的授权专利为ZL200680025545.1。
在不考虑专利期调整等因素时,PCT/US2006/011417专利家族至少将于2026年5月到期。
治疗用途家族
2012年7月,Medivation公司和科罗拉多大学共同递交了PCT国际专利申请(PCT/US2012/048471),权利要求涉及enzalutamide用于治疗三阴性乳腺癌的方法。目前,一项enzalutamide治疗三阴性乳腺癌的二期临床试验正在进行。
2016年8月,Medivation公司和安斯泰来公司共同递交了涉及enzalutamide与CYP3A4诱导剂联用治疗癌症的PCT专利申请(PCT/US2016/046476),同时要求2项美国的优先权。
可以看出,enzalutamide的专利策略是首先对结构通式进行限定,在最大范围内保护了所有可能成药的化合物。然后采用分案或延续案的方式进行更加精准的保护,限定要保护的化合物结构及可能的具体适应症,以增加对产品的保护。
晶型专利家族
在活性成分和治疗用途家族之后,安斯泰来公司于2016年5月还递交了涉及enzalutamide晶型的专利申请PCT/JP2016/065729, 其权利要求1涉及enzalutamide晶型的制备方法,限定了结晶步骤和湿晶干燥步骤,涉及使用不同比例的溶剂析晶; PCT/JP2016/065729的从属权利要求分别限定了多种常见有机溶剂,为其日后进一步优化药物晶型、争夺研发热点奠定基础。 目前 PCT/JP2016/065729已经进入中国国家阶段,仍处于审查阶段。
制剂专利家族
2013年9月,Medivation公司和安斯泰来公司共同递交了涉及enzalutamide制剂的PCT专利申请(PCT/US2013/059223)。独立权利要求涉及enzalutamide的无定形形式或包含无定形enzalutamide的一种固体制剂。
PCT/US2013/059223进入JP国家阶段的申请已经获得了授权—JP6404217B2,同时要求了一项美国的优先权(2012年9月)。权利要求保护无定形的enzalutamide或其制备方法。
安斯泰来公司改善了enzalutamide溶解度和口服生物利用度,2018年5月,递交了涉及enzalutamide制剂的PCT专利申请(PCT/JP2018/017159),同时要求了一项日本的优先权。权利要求涉及含有聚乙烯醇的enzalutamide的口服片剂或其制备方法。目前PCT/JP2018/017159尚未进入国家阶段。
可以看出,安斯泰来不断优化剂型以提高其口服生物利用度,并申请了多个相关专利家族,为日后进行剂型改进奠定了基础,并为竞争对手也设置了多重障碍。
结语
发明专利的权利保护类型分为产品和方法两类。围绕Xtandi的专利保护首先从产品的专利保护开始限定其结构,后续进一步针对其产品的制备方法、适应症、药物剂型、晶型结构等所有可能的改进点进行专利保护,构建起围绕enzalutamide的专利壁垒,这些专利资产为其进行产品升级优化提供独占权利,从而尽可能延长其生命周期。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
